题目内容
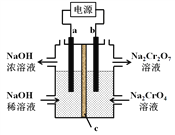
【题目】采用电解法还原CO2是CO2资源化的一种方法。某学习小组设计了一套以CO2为原料制备ZnC2O4的装置,其反应原理示意图如下(电解液不参与电极反应)。下列说法正确的是
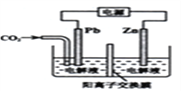
A. 电源的正极应与Pb电极连接
B. 电解时Zn2+可通过阳离子交换膜进入左侧
C. 电解时,阴极反应为:Zn-2e-═Zn2+
D. 标况下,消耗CO2气体4.48L时,交换膜右侧电解液质量减轻6.5g
【答案】B
【解析】采用电化学法还原CO2制备ZnC2O4的过程中,碳元素的化合价降低,所以通入二氧化碳的电极是阴极,即Pb是阴极,和电源的负极相连,Zn是阳极,和电源的正极相连,总反应为:2C02+Zn ![]() ZnC2O4。A、采用电化学法还原CO2制备ZnC2O4的过程中,碳元素的化合价降低,所以通入二氧化碳的电极是阴极,即Pb是阴极,和电源的负极相连,故A错误; B. Zn是阳极,电解时Zn2+可通过阳离子交换膜进入左侧,故B正确;C. 通入二氧化碳的电极是阴极,电解时,阴极上是二氧化碳得到电子生成草酸根离子,故C错误;D. 根据总反应,消耗标况下4.48L CO2气体,物质的量为
ZnC2O4。A、采用电化学法还原CO2制备ZnC2O4的过程中,碳元素的化合价降低,所以通入二氧化碳的电极是阴极,即Pb是阴极,和电源的负极相连,故A错误; B. Zn是阳极,电解时Zn2+可通过阳离子交换膜进入左侧,故B正确;C. 通入二氧化碳的电极是阴极,电解时,阴极上是二氧化碳得到电子生成草酸根离子,故C错误;D. 根据总反应,消耗标况下4.48L CO2气体,物质的量为![]() =0.2mol,交换膜右侧电极溶解0.1mol锌,有0.1molZn2+进入左侧,右侧电解液质量基本不变,故D错误;故选B。
=0.2mol,交换膜右侧电极溶解0.1mol锌,有0.1molZn2+进入左侧,右侧电解液质量基本不变,故D错误;故选B。

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目