题目内容
1.分类是化学学习和研究的常用方法之一.下列物质的分类正确的是( )| A. | 生石灰是氧化物 | B. | 甲烷属于电解质 | C. | 纯碱属于碱 | D. | 铝是常用氧化剂 |
分析 A、氧化物是由两种元素构成,其中一种是氧元素的化合物;
B、电解质是再水溶液或是熔融状态下能导电的化合物;
C、纯碱Na2CO3是盐不是碱;
D、金属元素无负价,故金属单质只能做还原剂.
解答 解:A、氧化物是由两种元素构成,其中一种是氧元素的化合物,故CaO是氧化物,故A正确;
B、甲烷是有机物,属于非电解质,故B错误;
C、纯碱Na2CO3是盐不是碱,故C错误;
D、金属元素无负价,故金属单质只能做还原剂,故D错误.
故选A.
点评 本题考查了氧化物、碱、电解质等的概念,难度不大,掌握概念是关键

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.将过量S02通入下列溶液中,能出现白色浑浊的是( )
①Ca (OH)2;②BaCl2;③Na[Al(OH)4];④Na2Si03;⑤Ba (NO3)2;⑥苯酚钠;⑦Na2CO3.
①Ca (OH)2;②BaCl2;③Na[Al(OH)4];④Na2Si03;⑤Ba (NO3)2;⑥苯酚钠;⑦Na2CO3.
| A. | ①②④⑦ | B. | ②③⑥⑦ | C. | ④⑤⑥⑦ | D. | ③④⑤⑥ |
12.X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)Y位于元素周期表第三周期VI族,Y和Z的最高价氧化物对应的水化物的酸性较强的是HClO4(写化学式).
(2)XY2是一种常用的溶剂,XY2的分子中存在2个σ键,X的杂化轨道类型是sp,XY2的分子的空间构形为直线形.在H-Y、H-Z两种共价键中,键长较长的是H-S.
(3)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1.
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.
已知:
XO(g)+0.5O2(g)=XO2(g)△H=-283.0kJ/mol
Y(g)+O2(g)=YO2(g)△H=-296.0kJ/mol
此反应的热化学方程式是2CO(g)+SO2(g)=2CO2(g)+S(g)△H=-270kJ/mol.
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(2)XY2是一种常用的溶剂,XY2的分子中存在2个σ键,X的杂化轨道类型是sp,XY2的分子的空间构形为直线形.在H-Y、H-Z两种共价键中,键长较长的是H-S.
(3)W的基态原子核外电子排布式是1s22s22p63s23p63d104s1.
(4)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y.
已知:
XO(g)+0.5O2(g)=XO2(g)△H=-283.0kJ/mol
Y(g)+O2(g)=YO2(g)△H=-296.0kJ/mol
此反应的热化学方程式是2CO(g)+SO2(g)=2CO2(g)+S(g)△H=-270kJ/mol.
9.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).

(1)制备氯气选用的药品为漂粉精固体和浓盐酸,相关反应的化学方程式为Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
(2)实验装置中B的作用是除氯气中的氯化氢,安全瓶作用.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入物质的组合是d(填编号).
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性.反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是E中溶液分为两层,上层(苯层)为紫红色.
(5)装置F中发生反应的离子方程式为Cl2+SO32-+H2O=SO42-+2H+. 若亚硫酸钠溶液中的亚硫酸钠已有4%发生变质,则吸收336mL氯气,至少需要1mol•L-1的此亚硫酸钠溶液156mL.

(1)制备氯气选用的药品为漂粉精固体和浓盐酸,相关反应的化学方程式为Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
(2)实验装置中B的作用是除氯气中的氯化氢,安全瓶作用.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入物质的组合是d(填编号).
| 编号 | a | b | c | d |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(5)装置F中发生反应的离子方程式为Cl2+SO32-+H2O=SO42-+2H+. 若亚硫酸钠溶液中的亚硫酸钠已有4%发生变质,则吸收336mL氯气,至少需要1mol•L-1的此亚硫酸钠溶液156mL.
16.下列反应既符合图象Ⅰ又符合图象Ⅱ的是( )


| A. | N2(g)+3H2(g)?2NH3(g)△H<0 | B. | 2SO3(g)?2SO2(g)+O2(g)△H>0 | ||
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H<0 | D. | C(s)+H2O(g)?H2(g)+CO(g)△H>0 |
6.下列中和反应的离子程式能以H++OH-═H2O表示的是( )
| A. | 醋酸和氢氧化钠溶液 | B. | 氢氧化镁和硝酸 | ||
| C. | 硫酸氢钠溶液和NaOH | D. | 氢氧化钡和稀硫酸 |
13.下列说法正确的是( )
| A. | 用玻璃棒蘸取某未知溶液进行焰色反应,若火焰颜色为黄色则说明一定有钠元素 | |
| B. | 某未知溶液加稀氢氧化钠溶液,未产生能使湿润红色石蕊试纸变蓝的气体,则说明原溶液不含NH${\;}_{4}^{+}$ | |
| C. | 某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- | |
| D. | 某溶液加入盐酸,无明显现象,再加BaCl2溶液,产生白色沉淀,则说明溶液中一定有 SO${\;}_{4}^{2-}$ |
2.CoCl2•6H2O在饲料、医药工业上有广泛的用途.下列是以含钴废料(含少量Fe、Al等杂质)为原料制取CoCl2•6H2O的一种新工艺流程如图1:
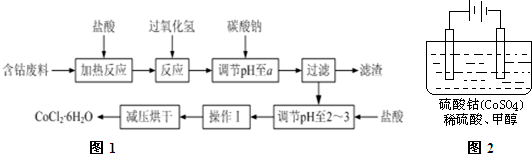
已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)加入碳酸钠调节pH至a,a的范围是5.2~7.6.
(2)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(3)制得的CoCl2•6H2O需减压烘干的原因是降低烘干温度,防止产品分解.
(4)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为减少有毒气体的排放,防止大气污染、防止产品中混有硝酸盐.原工艺较新工艺也有优点,其主要优点是流程的步骤减小,工艺减化.
(5)含钴物质在工业上有重要用途,有一种电化学法除去甲醇的污染,其原理是:通电后将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中甲醇氧化成CO2而净化.实验室用如图2装置模拟上述过程:
①写出阳极电极反应式Co2+-e-=Co3+.
②除去甲醇的离子反应为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+,该过程中被氧化的元素是碳元素,当生产过程中产生标况下2.24LCO2时,共转移电子数为3.612×1023.

已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.7 | 7.5 | 7.6 | 3.8 |
| 完全沉淀 | 3.2 | 9.7 | 9.2 | 5.2 |
(1)加入碳酸钠调节pH至a,a的范围是5.2~7.6.
(2)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(3)制得的CoCl2•6H2O需减压烘干的原因是降低烘干温度,防止产品分解.
(4)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为减少有毒气体的排放,防止大气污染、防止产品中混有硝酸盐.原工艺较新工艺也有优点,其主要优点是流程的步骤减小,工艺减化.
(5)含钴物质在工业上有重要用途,有一种电化学法除去甲醇的污染,其原理是:通电后将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中甲醇氧化成CO2而净化.实验室用如图2装置模拟上述过程:
①写出阳极电极反应式Co2+-e-=Co3+.
②除去甲醇的离子反应为:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+,该过程中被氧化的元素是碳元素,当生产过程中产生标况下2.24LCO2时,共转移电子数为3.612×1023.