题目内容
16.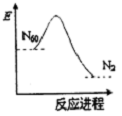 最近科学家确认,存在着一种具有空心,且类似于足球结构的分子N60,N60转化N2的能量变化如图所示.下列说法正确的是( )
最近科学家确认,存在着一种具有空心,且类似于足球结构的分子N60,N60转化N2的能量变化如图所示.下列说法正确的是( )| A. | N60转化N2是物理变化 | B. | N2不如N60稳定 | ||
| C. | N60转化N2是吸收能量的过程 | D. | N60可能成为一种好的火箭材料 |
分析 A、N60和N2是2种不同的物质;
B、当反应物的能量高于生成物的能量,反应是放热,能量越高越不稳定;
C、当反应物的能量高于生成物的能量,反应是放热;
D、根据当反应物的能量高于生成物的能量,反应是放热分析.
解答 解:A、N60和N2是2种不同的物质,所以N60转化N2是化学变化,故A错误;
B、从图中看出:氮气能量低稳定,所以N2比N60稳定,故B错误;
C、从图中看出:反应物的能量高于生成物的能量,所以反应是放热的,所以N60转化N2是放热的过程,故C错误;
D、从图中看出:反应物的能量高于生成物的能量,所以反应是放热的,则N60可能成为一种好的火箭材料,故D正确.
故选D.
点评 本题涉及物质的能量和反应的吸放热之间的关系,注意能量越高越不稳定,难度不大.

练习册系列答案
相关题目
6.下列关于金属腐蚀与防护的说法正确的是( )
| A. | 纯银器表面在干燥空气中因电化学腐蚀渐渐变暗 | |
| B. | 在海轮外壳连接锌块是采用了牺牲阳极的阴极保护法 | |
| C. | 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 | |
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
7.已知X、Y和Z三种元素的原子序数之和等于42.X元素原子的4p轨道上有3个未成对电子,Y元素原子的2p轨道上有2个未成对电子,X跟Y可形成化合物X2Y3,Z元素可形成正一价离子.下列说法正确的是( )
| A. | Y元素的基态原子核外原子排布式为1s22s22p2 | |
| B. | Y元素与Z元素可以形成化合物Z2Y2 | |
| C. | X元素的基态原子中3个未成对电子的能量不相同 | |
| D. | X元素与Z元素可以形成离子化合物XZ3 |
11.下列说法正确的是( )
| A. | SiH4比PH3稳定 | |
| B. | 短周期元素形成离子后,最外层电子都达到8电子稳定结构 | |
| C. | Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 | |
| D. | 某元素原子最外层只有一个电子,它跟卤素结合时所形成的化学键一定是离子键 |
1.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使石蕊变红色的溶液:Mg2+、K+、SO42-、NO3- | |
| B. | 使pH试纸呈深蓝色的溶液:Na+、Ba2+、HCO3-、NO3- | |
| C. | 0.1 mol•L-1AgNO3 溶液:H+、K+、SO42-、Br- | |
| D. | 0.1 mol•L-1 FeCl3溶液:H+、Na+、I-、SO42- |
8.下列物质中不能与金属钠反应的是( )
| A. | 苯 | B. | 水 | C. | 氧气 | D. | 乙醇 |
5.某芳香族化合物的分子式为C8H6O2,它的分子(除苯环外不含其他环)中不可能有( )
| A. | 一个醛基 | B. | 一个羧基 | C. | 两个羟基 | D. | 两个醛基 |
6. 研究人员通过对北京地区PM2.5的化学组成研究发现,汽车尾气和燃煤污染分别占4%、18%.
研究人员通过对北京地区PM2.5的化学组成研究发现,汽车尾气和燃煤污染分别占4%、18%.
(1)用稀土等催化剂能将汽车尾气中的CO、NOx碳氢化合物转化成无毒物质,从而减少汽车尾气传染.已知:
N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1
2C(s)+O2(g)=2CO(g)△H=-221.0kJ•mol-1
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1
写出NO(g)与CO(g)催化转化成N2(g)和CO2(g)的热化学方程式:2NO (g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5 kJ/mol.
(2)还可以用活性炭还原法处理氮氧化物,反应为C(s)+2NO(g)?N2(g)+CO2(g)H.向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
①T1℃时,该反应的平衡常数K=0.25(保留两位小数).
②前10min内用v(NO)表示的化学反应速率为0.0042mol/(L.min);30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是降低CO2浓度.
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2浓度之比为3:1:1,则该反应的△H<0(填“>”“=”或“<”).
(3)①用气体传感器可以检测汽车尾气中CO的含量.传感器是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.a为负极,电极反应式为CO-2e-+O2-═CO2.电池工作过程中,O2-由b极(填“a”或“b”,下同)移向a极.
②欧IV型汽车认证和生产一致性排放限值:汽油机CO1.00g/km.某测试车检测过程中,每行驶1km传感器中通过电子为0.08mol,则该车不符合(填“符合”或“不符合”)欧IV排放标准.
 研究人员通过对北京地区PM2.5的化学组成研究发现,汽车尾气和燃煤污染分别占4%、18%.
研究人员通过对北京地区PM2.5的化学组成研究发现,汽车尾气和燃煤污染分别占4%、18%.(1)用稀土等催化剂能将汽车尾气中的CO、NOx碳氢化合物转化成无毒物质,从而减少汽车尾气传染.已知:
N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-1
2C(s)+O2(g)=2CO(g)△H=-221.0kJ•mol-1
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1
写出NO(g)与CO(g)催化转化成N2(g)和CO2(g)的热化学方程式:2NO (g)+2CO(g)=N2(g)+2CO2(g)△H=-746.5 kJ/mol.
(2)还可以用活性炭还原法处理氮氧化物,反应为C(s)+2NO(g)?N2(g)+CO2(g)H.向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.050 | 0.025 | 0.025 |
| 30 | 0.050 | 0.025 | 0.025 |
| 40 | 0.036 | 0.032 | 0.010 |
| 50 | 0.036 | 0.032 | 0.010 |
②前10min内用v(NO)表示的化学反应速率为0.0042mol/(L.min);30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是降低CO2浓度.
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2浓度之比为3:1:1,则该反应的△H<0(填“>”“=”或“<”).
(3)①用气体传感器可以检测汽车尾气中CO的含量.传感器是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.a为负极,电极反应式为CO-2e-+O2-═CO2.电池工作过程中,O2-由b极(填“a”或“b”,下同)移向a极.
②欧IV型汽车认证和生产一致性排放限值:汽油机CO1.00g/km.某测试车检测过程中,每行驶1km传感器中通过电子为0.08mol,则该车不符合(填“符合”或“不符合”)欧IV排放标准.
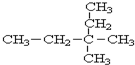 3,3-二甲基戊烷.
3,3-二甲基戊烷. .再将反应后的混合物转移到分液漏斗中,振荡、静置,然后分液.从分液漏斗放出下层液体,加入适量盐酸,再将其分成两份:向一份溶液中加入三氯化铁溶液,出现的现象是溶液呈紫色;向另一份溶液中加入浓溴水,反应的化学方程式为
.再将反应后的混合物转移到分液漏斗中,振荡、静置,然后分液.从分液漏斗放出下层液体,加入适量盐酸,再将其分成两份:向一份溶液中加入三氯化铁溶液,出现的现象是溶液呈紫色;向另一份溶液中加入浓溴水,反应的化学方程式为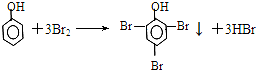 .从分液漏斗上口倒出的液体是苯.
.从分液漏斗上口倒出的液体是苯.