题目内容
7.下列物质分类正确的是( )| A. | 稀豆浆、雾、淀粉溶液、硫酸铜溶液均为胶体,也为混合物 | |
| B. | SO2、H2O、CO、CO2均为酸性氧化物,也为非金属氧化物 | |
| C. | 干冰、氨气、冰水混合物均为纯净物,也为化合物 | |
| D. | 凡是溶于水后能电离出H+的化合物就叫酸 |
分析 A、根据胶体、溶液等的定义和常见物质判断;
B、和碱反应生成盐和水的化合物为酸性氧化物;
C、同种物质组成的为纯净物,不同元素组成的纯净物为化合物;
D、盐溶液中也可以电离出氢离子.
解答 解:A、稀豆浆、雾、淀粉溶液为胶体,硫酸铜溶液属于溶液,故A错误;
B、SO2,CO2均和碱反应生成盐和水,为酸性氧化物,但是H2O、CO属于不成盐氧化物,故B错误;
C、干冰、氨气、冰水混合物均为纯净物,也为化合物,故C正确;
D、溶于水后能电离出H+的化合物不一定叫酸,如NaHSO4溶液中电离出氢离子,但属于盐,故D错误;
故选C.
点评 本题考查混合物、化合物、酸、氧化物的分类等概念,注意掌握物质组成和结构,题目较为简单,学习中注意对概念的理解要准确.

练习册系列答案
相关题目
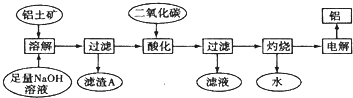
18.实验室用废CuO(含有杂质FeO、Fe2O3)制备胆矾晶体,经历下列过程(Fe3+在pH=5时已完全沉淀):下列分析正确的是( )


| A. | 用98%的浓硫酸配制溶解所用的4.5mol•L-1的稀硫酸,只需3种玻璃仪器 | |
| B. | 步骤②目的是将溶液Ⅰ中的Fe2+充分转化成Fe3+,实验操作是向溶液Ⅰ中通入足量的氯气 | |
| C. | 步骤④之后的实验操作是蒸干溶剂结晶,所需仪器是蒸发皿、泥三角、三脚架 | |
| D. | 利用Cu(OH)2 替代CuO也可调节溶液pH而不影响实验结果 |
15.在足量锌与2mol/L的盐酸反应中,为了加快反应的速率但又不改变产生的H2的总量,下列方法中可行的是( )
| A. | 加热 | B. | 加入少量的CuSO4溶液 | ||
| C. | 再加入一些3 mol/L的盐酸 | D. | 把锌粒改成更大块的 |
2.在标况下,一个装满Cl2的容器质量为74.6克;若装满N2则重为66克,那么此容器的容积为( )
| A. | 22.4升 | B. | 44.8升 | C. | 11.2升 | D. | 4.48升 |
12.下列变化需要加入氧化剂才能实现的是:( )
| A. | H2SO4→H2 | B. | Fe2+→Fe3+ | C. | O2→H2O | D. | HNO3→NO2 |
17.已知反应:2SO2(g)+O2(g)?2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)、温度(T)等条件的变化关系如下图所示.则下列说法正确的是( )
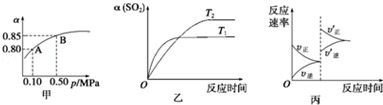

| A. | 由图甲知,A点SO2的平衡浓度为0.4 mol/L | |
| B. | 由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2 | |
| C. | 压强为0.50 MPa时不同温度下SO2转化率与温度关系如图乙,则T2>T1 | |
| D. | 达平衡后,缩小容器容积,则反应速率变化图象可以用图丙表示 |