题目内容
17.下列反应原理中,不符合工业冶炼金属实际情况的是( )| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | 2Al+3MnO2$\frac{\underline{\;高温\;}}{\;}$2Al2O3+3Mn | ||
| C. | 2MgO$\frac{\underline{\;电解\;}}{\;}$2Mg+O2↑ | D. | 4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 |
分析 金属的性质不同,活泼性不同,冶炼的方法不同,根据金属活动性强弱,可采用热还原法、电解法、热分解法等冶炼方法.
热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来,例如:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑
热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来,例如:
Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+CO2↑
电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属,例如:
2Al2O3 $\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑
利用铝热反应原理还原:V、Cr、Mn、W等高熔点金属可利用铝热反应产生的高温来冶炼.
解答 解:A.Hg是不活泼金属,采用直接加热分解其氧化物的方法冶炼,故A正确;
B.Mn的金属性小于Al,且熔点大于Al,所以V、Cr、Mn、W等高熔点金属可利用铝热反应产生的高温来冶炼,故B正确;
C.Mg是活泼金属,MgO熔点较高、氯化镁熔点较低,所以工业上为减少资源消耗,采用电解熔融氯化镁方法冶炼镁,故C错误;
D.在金属活动性顺序表中Fe是处于中间位置的金属,通常是用还原剂将Fe从其化合物中还原出来,故D正确;
故选C.
点评 本题考查金属冶炼,明确金属活泼性强弱与冶炼方法的关系是解本题关键,根据金属活泼性强弱选取合适的冶炼方法,易错选项是C.

练习册系列答案
相关题目
7.钠与下列物质反应都能够产生氢气:①H2O;②CH3COOH;③CH3CH2OH 试推断这三种物质电离出H+的难易程度(从难到易的顺序)( )
| A. | ①②③ | B. | ②③① | C. | ③①② | D. | ②①③ |
8.下列说法不正确的是( )
| A. | 进行分液操作时,应先打开上口活塞或使塞上的凹槽对准漏斗口的小孔,然后打开旋塞,下层液体从下口放出,上层液体从漏斗上口倒出 | |
| B. | 纸层析法是以滤纸为惰性支持物,水为固定相,有机溶剂作流动相.用该方法可分离Fe3+和Cu2+,层析后氨熏显色,滤纸上方出现红棕色斑点 | |
| C. | 酸式滴定管、碱式滴定管、容量瓶、移液管都是准确量取一定体积液体的容器,它们在使用时都要进行检查是否漏水、水洗、润洗、注液、调整液面等几个过程 | |
| D. | 在制备硝酸钾晶体的实验中,趁热过滤时,承接滤液的小烧杯中预先加2mL蒸馏水.以防过滤时氯化钠晶体析出 |
5.下列不属于有机物的是( )
| A. | 氯化钠 | B. | 醋酸 | C. | 乙炔 | D. | 尿素 |
12.实验室制备少量硫酸亚铁晶体的实验步骤如下:①趁热过滤 ②洗涤、滤纸吸干 ③静置、冷却④水浴加热⑤抽滤 ⑥过量铁屑,加入20%-30%的稀硫酸溶液.则实验步骤正确的顺序为( )
| A. | ⑥⑤④①③② | B. | ⑥④⑤②①③ | C. | ⑥④①③⑤② | D. | ②⑥④①③⑤ |
2.用氯丙醛(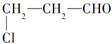 )制取聚丙烯酸(
)制取聚丙烯酸(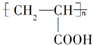 )的过程中发生的反应类型为( )
)的过程中发生的反应类型为( )
①取代 ②消去 ③加聚 ④还原 ⑤氧化.
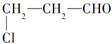 )制取聚丙烯酸(
)制取聚丙烯酸(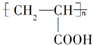 )的过程中发生的反应类型为( )
)的过程中发生的反应类型为( )①取代 ②消去 ③加聚 ④还原 ⑤氧化.
| A. | ⑤①②③ | B. | ⑤②③ | C. | ①②⑤③ | D. | ②③⑤④ |
9.下说法正确的是( )
| A. | 从海水中提取溴,富集溴可以用亚硫酸钠溶液或二氧化硫水溶液作为吸收液 | |
| B. | 从海水中提取碘常用过氧化氢做还原剂 | |
| C. | 可以用铝热反应制得单质镁 | |
| D. | 铝热剂就是指铝和氧化铁混合物 |
6.一定温度下,反应N2(g)+3H2(g)?2NH3(g)达到化学平衡状态的标志是( )
| A. | c(N2):c(H2):c(NH3)=1:3:2 | |
| B. | N2、H2和NH3的质量分数不再改变 | |
| C. | N2与H2的物质的量之和是NH3的物质的量的2倍 | |
| D. | 单位时间里每增加1 mol N2,同时减少2 mol NH3 |
14.下列说法正确的是( )
| A. | 丙烯酸和油酸互为同系物 | |
| B. | 淀粉和纤维素互为同分异构体 | |
| C. | CuSO4浓溶液能使蛋白质溶液发生盐析 | |
| D. | 麦芽糖和脂肪在一定条件下都能发生水解反应 |