题目内容
6.一定温度下,反应N2(g)+3H2(g)?2NH3(g)达到化学平衡状态的标志是( )| A. | c(N2):c(H2):c(NH3)=1:3:2 | |
| B. | N2、H2和NH3的质量分数不再改变 | |
| C. | N2与H2的物质的量之和是NH3的物质的量的2倍 | |
| D. | 单位时间里每增加1 mol N2,同时减少2 mol NH3 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、当体系达平衡状态时,c(N2):c(H2):c(NH3)可能为1:3:2,也可能不是,与各物质的初始浓度及转化率有关,故A错误;
B、N2、H2和NH3的质量分数不再改变,正逆反应速率相等,各组分的量不变,说明达平衡状态,故B正确;
C、当体系达平衡状态时,N2与H2的物质的量之和可能是NH3的物质的量的2倍,也可能不是2倍,与各物质的初始浓度及转化率有关,故C错误;
D、都体现的是逆向,未体现正与逆的关系,故D错误;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
17.下列反应原理中,不符合工业冶炼金属实际情况的是( )
| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | 2Al+3MnO2$\frac{\underline{\;高温\;}}{\;}$2Al2O3+3Mn | ||
| C. | 2MgO$\frac{\underline{\;电解\;}}{\;}$2Mg+O2↑ | D. | 4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 |
1.某草药中有一种色素,它的结构简式为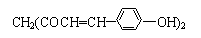 ,用它制成的试剂可以检验物质的酸碱性.能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是( )
,用它制成的试剂可以检验物质的酸碱性.能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是( )
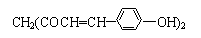 ,用它制成的试剂可以检验物质的酸碱性.能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是( )
,用它制成的试剂可以检验物质的酸碱性.能够跟1mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是( )| A. | 3 mol、5 mol | B. | 6 mol、8 mol | C. | 10 mol、8 mol | D. | 6 mol、10 mol |
11.下列化学式表示的物质一定为纯净物的是( )
| A. | C3H8 | B. | C4H10 | C. | C12H22O11 | D. | C |
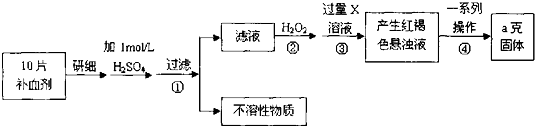
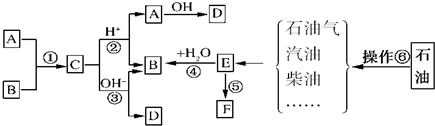
 .
.
 .
.
 .
.