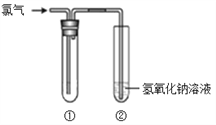
��Ŀ����
����Ŀ��ľ̿������̿��̿�ڡ���̿����ʯī��С������������ʹ��ɵģ���������û�й̶��ļ������Σ����Գ�Ϊ����̼���ڹ�ҵ��������Ҫ��;���ش��������⣺
��1��ľ̿����ơ�����������أ���һ��������ϼ�Ϊ�ڻ�ҩ���ڻ�ҩ��ըʱ�����ء������Ͷ�����̼���ڻ�ҩ��ը�Ļ�ѧ����ʽΪ____________������15gľ̿�μӷ�Ӧ��ת�Ƶ�����Ϊ____________��
��2����ҵ�ϵ�̿�����������ѽ���Ƶõĸ߶ȷ�ɢ�Եĺ�ɫ��ĩ״���ʡ�
����֪������Ӧ���Ȼ�ѧ����ʽ��
C(s)+O2 (g)CO2(g) ��H1=393.5 kJmol1
2H2(g)+O2 (g)2H2O(1) ��H2=571.6 kJmol1
CH4(g)+2O2(g)CO2(g)+ 2H2O(1) ��H3=890.3 kJmol1
������Ȼ������̿�ڵ��Ȼ�ѧ����ʽΪ____________��
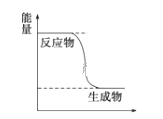
����ͼ���¶ȶ���Ȼ������̿��ת���ʵ�Ӱ���������й�˵����ȷ����____________��
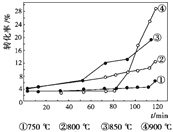
A. �����ѽ��������ȷ�Ӧ
B. ������ϵѹǿ����������ת����
C. �ڷ�Ӧ��ϵ�мӴ�������Ӧ��������
D. �����¶ȣ��÷�Ӧ��ƽ�ⳣ����С
��3������̿�����������������Һ�塣
���û���̿��ԭ��������ɷ�ֹ������Ⱦ����1 L�ܱ���������һ�����Ļ���̿��NO��ij�¶��·�����ӦC��s��+ 2NO��g��![]() N2��g��+CO2��g������ò�ͬʱ���ڸ����ʵ����ʵ������±���
N2��g��+CO2��g������ò�ͬʱ���ڸ����ʵ����ʵ������±���
���ʵ���/mol ʱ��/min | NO | N2 | CO2 |
0 | 0.200 | 0 | 0 |
10 | 0.116 | 0.042 | 0.042 |
20 | 0.080 | 0.060 | 0.060 |
30 | 0.080 | 0.060 | 0.060 |
���¶��£��÷�Ӧ��ƽ�ⳣ��K=____________ (������λС��)��10~20min�ڣ�NO��ƽ����Ӧ����Ϊ____________����30 min�������¶ȣ��ﵽ��ƽ��ʱ��������c(NO)��c(N2)��c(CO2)=2��1��1����÷�Ӧ����H____________0(����>������<������=��)��
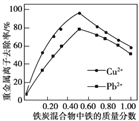
�ڻ���̿����м��Ͽ����ڴ���ˮ����Ⱦ�����ͬ�����£�������������ͬ����������������ͬ����̿������ˮ��span>Cu2+��Pb2+��ȥ���ʣ������ͼ��ʾ�����������������������Ϊ0ʱ��Ҳ��ȥ��ˮ��������Cu2+��Pb2+����ԭ����____________���������������������������50%ʱ�����������������������ӣ�Cu2+��Pb2+��ȥ���ʲ�������������Ҫԭ����____________��
���𰸡� 2KNO3+ S + 3C = K2S + N2��+3CO2�� 5NA CH4(g)C(s) +2H2(g) ��H =+74.8kJmol1 A C 0.56 0.0036molL1min1 �� ����̿��Cu2+��Pb2+���������� ̿�������������٣�������������Ŀ����
��������(1)������Ŀ�����ɵã��ڻ�ҩ��ը�Ļ�ѧ����ʽΪ2KNO3+ S + 3C = K2S + N2��+3CO2����
�÷�Ӧ��3molC�μӷ�Ӧ��ת�Ƶ�������Ϊ12mol������15gľ̿�μӷ�Ӧ��ת�Ƶ�����Ϊ=![]() ��
��
(2) ����������Ӧ�ֱ�����٢ڢۣ����ɢ�-��-�ٿɵã�CH4(g)= C(s)+ 2H2(g) ��H=+74.8 kJmol1��
����ͼ���֪����Ȼ������̿�ڵ�ת�������¶����߶�����˵�������ѽ������ȷ�Ӧ����A��ȷ������һ�������������ķ�Ӧ����������ѹǿ����Ӧ��������У������ת�����ǽ��͵ģ���B�������ܼӿ췴Ӧ���ʣ����̴ﵽƽ���ʱ�䣬����C��ȷ�������ѽ���һ�����ȷ�Ӧ�����������¶ȣ�ƽ�������ƶ���ƽ�ⳣ��������ģ���D����������ȷ��ΪAC��
(3)��30���ӷ�Ӧ�Ѵ�ƽ�⣬��Ӧ��ƽ�ⳣ��K=![]() =0.56��10~20min�ڣ�NO��ƽ����Ӧ����Ϊ��(NO)=
=0.56��10~20min�ڣ�NO��ƽ����Ӧ����Ϊ��(NO)= ![]() 0.0036 mol/(Lmin)����30 min�������¶ȣ��ﵽ��ƽ��������c(NO)��c(N2)��c(CO2)=2��1��1����ʱK1=0.25<K=0.56�����������¶�ƽ�������ƶ�����÷�Ӧ��H<0�����Ƿ��ȷ�Ӧ��
0.0036 mol/(Lmin)����30 min�������¶ȣ��ﵽ��ƽ��������c(NO)��c(N2)��c(CO2)=2��1��1����ʱK1=0.25<K=0.56�����������¶�ƽ�������ƶ�����÷�Ӧ��H<0�����Ƿ��ȷ�Ӧ��
�ڻ���̿�����������ã���������������Cu2+��Pb2+����ȥ�����������������������ӣ�̿�����������ڼ��٣�һ��������̿�γɵ������Ŀ�ڼ��٣���һ�������̿����������Ҳ�����ˣ�����Cu2+��Pb2+��ȥ���ʲ���������

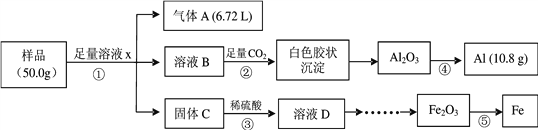
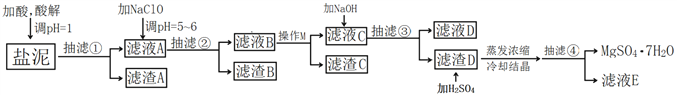
����Ŀ����ҵ�������ȼҵ�еĹ���������ࣨ��Ҫ�ɷ�ΪMg(OH)2��CaCO3��BaSO4������֮���NaCl��Al(OH)3��Fe(OH)3��Mn(OH)2�ȡ������ϡ���ᷴӦ�Ʊ���ˮ����þ�����ʸߣ��ȴ��������ϣ����о���Ч�档�乤���������£�
��֪��
i������������������������ʽ��ȫ����ʱ��Һ��pH
������ | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
pHֵ����ȫ������ | 10.02 | 8.96 | 3.20 | 4.70 | 11.12 |
ii�������ε��ܽ��ͼ����λΪg/100gˮ��
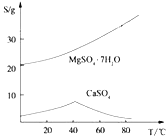
������������ͼ���ο�����pH���ݺ��ܽ��ͼ����ش��������⡣
��1�����ʱ���������Ϊ____________�����������У���ӿ�������ʣ���������ֿ��еĴ�ʩ____________��____________��
��2�������NaClO����Mn2+��Ӧ����MnO2�������÷�Ӧ�����ӷ���ʽ��____________��
��3�����������̶���õ����˲��������ŵ�����____________���Ĵγ���ʱ�����ˢ���������A�ijɷ�Ϊ____________��CaSO4�����ˢ���������B�ijɷ�ΪMnO2��____________��____________��������������ҺC����Ҫ���������ӵļ��鷽����____________�����ˢܽ���Ʒ��ɡ�
��4�������ܽ�����ߣ�����MӦ��ȡ�ķ������ʵ�Ũ����____________��
��5��ÿ�Ʊ�1��MgSO4��7H2O����Ҫ��������2�֡������������е�ת����Ϊ70%����������þ����������þ�ƣ�����������ԼΪ____________��