题目内容
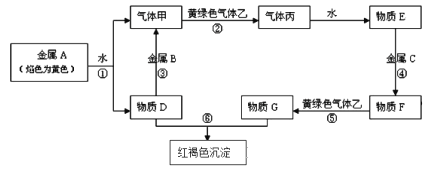
【题目】某研究小组利用废弃的铁铝混合物(含Fe、Al、Al2O3、Fe2O3)回收金属铝和铁,实验流程设计如下:
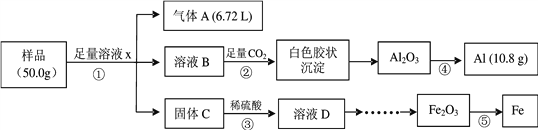
(1)写出①中发生反应的离子方程式___________、_____________。
(2)下列说法正确的是_________。
a. ②中发生的是非氧化还原反应
b. ③中所得溶液D中含有Fe2+和Fe3+
c. ④和⑤分别采用电解法和热还原法
(3)由溶液D制取Fe2O3的实验过程是 ______________。
(4)该样品中Al2O3的质量分数是_____________。
【答案】 2Al + 2OH- + 2 H2O = 2AlO2- +3H2↑ Al2O3 + 2OH- =2AlO2- + H2O abc 加入过量的氢氧化钠溶液,过滤,加热 20.4%
【解析】从实验流程可知,样品需加氢氧化钠溶液溶解Al和Al2O3,实现和Fe和Fe2O3的分离,则溶液x为氢氧化钠溶液,反应①为Al和氢氧化钠溶液反应生成偏铝酸钠和氢气,以及Al2O3和氢氧化钠溶液反应生成偏铝酸钠和水;溶液B为偏铝酸钠溶液,固体C为Fe和Fe2O3的混合物,反应②为偏铝酸钠溶液通入足量的二氧化碳,生成氢氧化铝沉淀,反应③为Fe和Fe2O3分别和稀硫酸反应所得D溶液中含有Fe2+和Fe3+,反应④为电解熔融Al2O3制取Al,反应⑤为热还原法炼铁的反应,以此分析。
结合以上分析,(1)写出①中发生反应的离子方程式2Al + 2OH- + 2H2O = 2AlO2- +3H2↑ 、Al2O3 + 2OH- =2AlO2- + H2O;
(2)a. ②中发生NaAlO2+CO2+2H2O==Al(OH)3↓+NaHCO3,属于非氧化还原反应,a正确;
b. ③中反应为Fe+H2SO4==FeSO4+H2↑、Fe2O3+ 3H2SO4==Fe2(SO4)3+3H2O,因此所得溶液D中含有Fe2+和Fe3+,b正确;c. 反应④是电解熔融Al2O3制取Al,反应⑤为热还原法炼铁的反应,故c正确;因此本题答案为:abc。
(3)由溶液D含有Fe2+和Fe3+,向溶液D中加入过量的氢氧化钠溶液,过滤,可转化为氢氧化铁沉淀,加热氢氧化铁分解生成Fe2O3。因此本题答案为:加入过量的氢氧化钠溶液,过滤,加热。
(4)从实验流程知,最终得到Al为10.8g;根据反应①中2Al + 2OH- + 2H2O = 2AlO2- +3H2↑,样品中的Al的质量为:![]() ×
×![]() ×27g/mol=5.4g;则样品中含Al2O3的质量为(10.8g-5.4g)×
×27g/mol=5.4g;则样品中含Al2O3的质量为(10.8g-5.4g)×![]() =10.2g,所以该样品中Al2O3的质量分数是
=10.2g,所以该样品中Al2O3的质量分数是![]() ×100%=20.4%。
×100%=20.4%。
因此本题答案为:20.4%。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】木炭、活性炭、炭黑、焦炭是由石墨的微小晶体和少量杂质构成的,均属混合物。没有固定的几何外形,所以称为无定形碳,在工业上有着重要用途。回答下列问题:
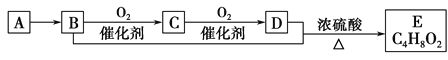
(1)木炭与硫黄、火硝(硝酸钾)按一定比例混合即为黑火药。黑火药爆炸时生成硫化钾、氮气和二氧化碳。黑火药爆炸的化学方程式为____________。若有15g木炭参加反应,转移电子数为____________。
(2)工业上的炭黑是由烃类裂解而制得的高度分散性的黑色粉末状物质。
①已知几个反应的热化学方程式:
C(s)+O2 (g)CO2(g) ΔH1=393.5 kJmol1
2H2(g)+O2 (g)2H2O(1) ΔH2=571.6 kJmol1
CH4(g)+2O2(g)CO2(g)+ 2H2O(1) ΔH3=890.3 kJmol1
则由天然气生产炭黑的热化学方程式为____________。
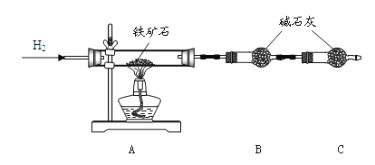
②右图是温度对天然气生产炭黑转化率的影响,下列有关说法正确的是____________。
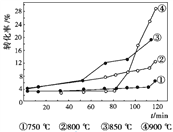
A. 甲烷裂解属于吸热反应
B. 增大体系压强,能提高甲烷的转化率
C. 在反应体系中加催化剂,反应速率增大
D. 升高温度,该反应的平衡常数减小
(3)活性炭可以用来净化气体和液体。
①用活性炭还原氮氧化物,可防止空气污染。向1 L密闭容器加入一定量的活性炭和NO,某温度下发生反应C(s)+ 2NO(g)![]() N2(g)+CO2(g),测得不同时间内各物质的物质的量如下表:
N2(g)+CO2(g),测得不同时间内各物质的物质的量如下表:
物质的量/mol 时间/min | NO | N2 | CO2 |
0 | 0.200 | 0 | 0 |
10 | 0.116 | 0.042 | 0.042 |
20 | 0.080 | 0.060 | 0.060 |
30 | 0.080 | 0.060 | 0.060 |
此温度下,该反应的平衡常数K=____________ (保留两位小数)。10~20min内,NO的平均反应速率为____________;若30 min后升高温度,达到新平衡时,容器中c(NO)∶c(N2)∶c(CO2)=2∶1∶1,则该反应的ΔH____________0(填“>”、“<”或“=”)。
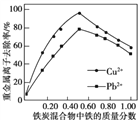
②活性炭和铁屑混合可用于处理水中污染物。在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中span>Cu2+和Pb2+的去除率,结果如图所示。当混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是____________;当混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是____________。