题目内容
【题目】聚合硫酸铁[Fe(OH)SO4]n能用作净水剂(絮凝剂),可由绿矾(FeSO47H2O)和KClO3在水溶液中反应得到。下列说法不正确的是( )
A.KClO3作氧化剂,每生成1mol[Fe(OH)SO4]n消耗![]() molKClO3
molKClO3
B.生成聚合硫酸铁后,水溶液的pH一定增大
C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
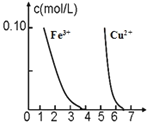
D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强
【答案】A
【解析】
A.KClO3作氧化剂氧化FeSO4生成[Fe(OH)SO4]n的化学方程式为6nFeSO4+nKClO3+3nH2O=6[Fe(OH)SO4]n+nKCl,所以每生成1mol [Fe(OH)SO4]n消耗![]() mol KClO3,故A选项错误。
mol KClO3,故A选项错误。
B:Fe2(SO4)3是强酸弱盐,水溶液显酸性,聚合硫酸铁又称为碱式硫酸铁,生成聚合硫酸铁后,水溶液的酸性减弱pH增大,故B选项正确。
C.聚合硫酸铁中的铁为+3价,能用作净水剂,则聚硫酸铁能水解生成氢氧化铁胶体,氢氧化铁胶体能吸附水中的悬浮物而净水,故C选项正确。
D.Fe3+为弱碱阳离子,水解也是分步进行,只是通常规定Fe3+的水解一步到位,所以Fe3+的水解第一步程度最大,即Fe3+比[Fe(OH)]2+的水解能力更强,故D选项正确。
故答案选A。

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目