题目内容
4.I.铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物.已知氯化铁是一种重要的化工原料,无水氯化铁遇潮湿空气极易吸水生成FeCl3•nH2O.
(1)某学习小组用如图1装置在实验室制备无水氯化铁,请你一起参与该小组的活动.
①装置A 中仪器 a的名称是分液漏斗.
②装置B的作用是除去氯气中的氯化氢,C 中的试剂浓硫酸.
③实验开始时先点燃A处酒精灯;装置 E的作用为阻止外界空气中的水蒸气进入D,吸收尾气.
(2)工业上制备无水氯化铁的一种工艺流程如下:
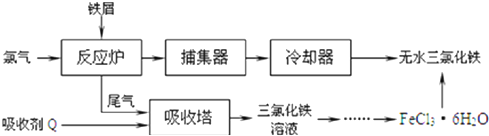
①吸收塔中发生反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-
②简述由FeCl3•6H2O晶体得到无水氯化铁的操作:在HCl气流中加热蒸干
II.利用如图2所示的装置,可以验证NH3和 HCl的有关性质.实验前a、b、c活塞均关闭.
(1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是先打开ab活塞,再挤压胶头滴管(或先挤压胶头滴管,再打开ab活塞)
(2)若先打开a、c 活塞,再挤压胶头滴管(假设NH3不被完全吸收),在烧瓶Ⅱ中可观察到的现象导管口处出现白烟-.
(3)通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是先打开ac活塞,再挤压胶头滴管(或先打开a活塞挤压胶头滴管,再打开c活塞),片刻后关a活塞,再打开b活塞.
分析 Ⅰ.(1)实验室制备无水氯化铁,需要先制取氯气,用A装置,根据题意B用于除去氯气中的氯化氢,C用于干燥氯气,由于无水氯化铁遇潮湿空气极易吸水生成FeCl3•nH2O,所以E防止空气中的水蒸气进入,同时吸收未反应的氯气,防止污染空气.实验时先点燃A处的酒精灯,使装置中充满氯气,再点燃D出的酒精灯,这样可以防止铁与氧气发生反应;
(2)氯气与铁在反应炉中反应生成氯化铁,尾气用吸收剂Q处理得到氯化铁,故Q为氯化亚铁,氯化铁溶液蒸发浓缩、冷却结晶得到氯化铁晶体,为防止氯化铁水解,在HCl气流中加热蒸干氯化铁晶体得到氯化铁;
Ⅱ.(1)若要在烧瓶Ⅱ中产生喷泉,先打开ab活塞,再挤压胶头滴管(或先挤压胶头滴管,再打开ab活塞),则在Ⅱ中氨气被水吸收形成负压;
(2)若先打开a、c 活塞,Ⅰ中氯化氢进入Ⅱ中,氯化氢和氨气反应生成固体氯化铵;
(3)要在烧瓶Ⅰ中形成喷泉,就要形成负压:先打开ac活塞,再挤压胶头滴管,Ⅰ中氯化氢部分进入Ⅱ中,使Ⅰ中形成负压,关a活塞,再打开b活塞.
解答 解:Ⅰ.实验室制备无水氯化铁,需要先制取氯气,用A装置,根据题意B用于除去氯气中的氯化氢,C用于干燥氯气,由于无水氯化铁遇潮湿空气极易吸水生成FeCl3•nH2O,所以E防止空气中的水蒸气进入,同时吸收未反应的氯气,防止污染空气.实验时先点燃A处的酒精灯,使装置中充满氯气,再点燃D出的酒精灯,这样可以防止铁与氧气发生反应.
(1)①装置A 中仪器 a的名称是:分液漏斗,
故答案为:分液漏斗;
②装置B的作用是:除去氯气中的氯化氢,C用于干燥氯气,C 中的试剂可以为:浓硫酸,
故答案为:除去氯气中的氯化氢;浓硫酸;
③实验开始时先点燃A处酒精灯;装置 E的作用为:阻止外界空气中的水蒸气进入D,吸收尾气,
故答案为:A;阻止外界空气中的水蒸气进入D,吸收尾气;
(2)氯气与铁在反应炉中反应生成氯化铁,尾气用吸收剂Q处理得到氯化铁,故Q为氯化亚铁,氯化铁溶液蒸发浓缩、冷却结晶得到氯化铁晶体,为防止氯化铁水解,在HCl气流中加热蒸干氯化铁晶体得到氯化铁.
①吸收塔中发生反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
②FeCl3•6H2O晶体得到无水氯化铁,应防止氯化铁水,需要在在HCl气流中加热蒸干,故答案为:在HCl气流中加热蒸干;
Ⅱ(1)若要在烧瓶Ⅱ中产生喷泉,先打开ab活塞,再挤压胶头滴管(或先挤压胶头滴管,再打开ab活塞),则在Ⅱ中氨气被水吸收形成负压,
故答案为:先打开ab活塞,再挤压胶头滴管(或先挤压胶头滴管,再打开ab活塞);
(2)若先打开a、c 活塞,Ⅰ中氯化氢进入Ⅱ中,氯化氢和氨气反应生成固体氯化铵,出现白烟,
故答案为:导管口处出现白烟;
(3)要在烧瓶Ⅰ中形成喷泉,就要形成负压:先打开ac活塞,再挤压胶头滴管,Ⅰ中氯化氢部分进入Ⅱ中,使Ⅰ中形成负压,关a活塞,再打开b活塞,
故答案为:先打开ac活塞,再挤压胶头滴管(或先打开a活塞挤压胶头滴管,再打开c活塞),片刻后关a活塞,再打开b活塞.
点评 本题考查制备实验方案设计、喷泉实验等,明确原理是解题关键,是对学生综合能力的考查,难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 甲苯 | B. | 金属Cu | C. | NaCl溶液 | D. | HCl溶液 |
| A. | 3:2 | B. | 2:3 | C. | 11:9 | D. | 1:3 |
| A. | 配制标准溶液的NaOH中混有Na2CO3杂质 | |
| B. | 滴定终点读数时,俯视滴定管的刻度,其他操作正确 | |
| C. | 盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗 | |
| D. | 滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液 |
| A. | Na2CO3固体 | B. | NaCl溶液 | C. | 浓H2SO4 | D. | KNO3溶液 |
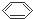 -OH)2用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )
-OH)2用它制成的试纸可以检验溶液的酸碱性.能够跟1mol该化合物起反应的Br2水溶液或H2的最大用量分别是( )| A. | 3 mol 3 mol | B. | 3 mol 5 mol | C. | 6 mol 6 mol | D. | 6 mol 10 mol |
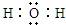 ,C和D形成的一种化合物与A2C发生氧化还原反应,该反应的离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑
,C和D形成的一种化合物与A2C发生氧化还原反应,该反应的离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑