题目内容
【题目】用锌片与稀硫酸反应制取氢气,下列措施不能使氢气的生成速率增大的是( )
A. 加热 B. 将锌片改成锌粉
C. 滴加少量CuSO4溶液 D. 加入适量Na2CO3粉末
【答案】D
【解析】
根据外因对反应速率的影响分析回答。
A项:加热升高温度,使反应加快;
B项:将锌片改成锌粉增大反应物的接触面积,使反应加快;
C项:滴加少量CuSO4溶液,CuSO4与锌发生置换反应生成Cu和ZnSO4,Cu、Zn与稀硫酸形成原电池,使反应加快;
D项:加入Na2CO3粉末消耗硫酸,降低了反应物浓度,使反应变慢。
本题选D。

 优化作业上海科技文献出版社系列答案
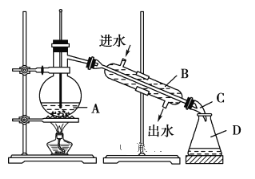
优化作业上海科技文献出版社系列答案【题目】葡萄酒中抗氧化剂的残留量是以游离SO2的含量计算,我国国家标准(GB2760-2014)规定葡萄酒中SO2的残留量≤0.25g/L。某兴趣小组用下图装置(夹持装置略)收集某葡萄酒中的SO2,并对含量进行测定。实验步骤如下

i. 检查装置的气密性后,向仪器A中加入300.00ml葡萄酒和适量盐酸
ii. 加热使SO2全部逸出并与B中H2O2完全反应
iii. 除去B中过量的H2O2后,将B中溶液取出,稀释至100mL
iv.取25.00mL 稀释后的溶液至于锥形瓶中,加入几滴酚酞
v.用0.0300mol/L NaOH标准溶液进行滴定,重复三次
(1)SO2在水中可形成SO2 ─饱和H2SO3溶液体系,此体系中存在多个含硫元素的平衡,分别用化学方程式表示为_______________。
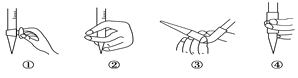
(2)图中①中仪器名称为_____________,步骤v中,滴定前排气泡时,应选择图中的___。
(3)除去过量H2O2的方法是_________________。
(4)滴定的终点现象_____________________________________;若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积 (填序号)___________(①=10 mL,②=40 mL,③<10 mL,④>40 mL)。
(5)滴定消耗的NaOH溶液的体积如下,则该葡萄酒中SO2含量为____g/L。
滴定次数 | 1 | 2 | 3 |
NaOH溶液体积/mL | 21.80 | 20.02 | 19.98 |
(6)某同学认为该测定结果不能说明该葡萄酒中SO2残留量一定超标。原因是__________。利用现有装置可以如何改进?_____________。