题目内容
【题目】氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2·2H2O)的主要流程如下:
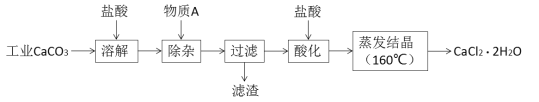
完成下列填空:
(1)除杂操作是加入物质A来调节溶液的pH,以除去溶液中的Al3+、Fe3+,根据下表所给信息,此时控制溶液的pH范围是_____________,加入的物质A是___________(写化学式)。
开始沉淀时的pH | 沉淀完全时的pH | 沉淀开始溶解时的pH | |
Al(OH)3 | 3.3 | 5.2 | 7.8 |
Fe(OH)3 | 1.5 | 4.1 | - |
(2)检验Fe3+是否沉淀完全的实验操作是____________________________________________。
(3)酸化操作是加入盐酸,调节溶液的pH,其目的是_________________________________。
(4)测定制得的样品的纯度,可采用如下方案:
a.称取0.750 g样品,溶解,在250 mL容量瓶中定容;
b.量取25.00 mL待测溶液于锥形瓶中;
c.用0.050 mol/L AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39 mL。
①上述测定过程中,需要用到的玻璃仪器除了容量瓶、锥形瓶,还有__________________。
②计算上述样品中CaCl2·2H2O的质量分数为__________________(保留三位有效数字)。
③若配制和滴定操作均无误,但最终测定的样品中CaCl2·2H2O的质量分数偏高,写出可能导致该结果的一种情况___________________________________________。
【答案】5.2≤pH<7.8 Ca(OH)2 或CaO或CaCO3 取少量上层清液,滴加KSCN溶液,若不出现血红色,表明Fe(OH)3沉淀完全 将溶液中的少量Ca(OH)2转化为CaCl2 烧杯、玻璃棒、胶头滴管、滴定管 99.9% 蒸发结晶过程中,温度过高,使CaCl2·2H2O失去部分结晶水
【解析】
工业碳酸钙加过量盐酸进行溶解,得到Ca2+、Al3+、Fe3+,加入物质A来调节溶液的pH,以除去溶液中的Al3+、Fe3+,根据沉淀对应的pH表,需要把二者沉淀完全,pH最小为5.2,但是当pH大于等于7.8,氢氧化铝开始溶解,故调节pH范围是5.2≤pH<7.8;加入的A能调节pH,但是不能引入新杂质,则可以选用Ca(OH)2 或CaO或CaCO3;过滤后滤液进行盐酸酸化,在160℃蒸发结晶,得产品CaCl2·2H2O。
(1)根据分析,加入物质A来调节溶液的pH,此时控制溶液的pH范围是5.2≤pH<7.8;加入的物质A是Ca(OH)2 或CaO或CaCO3(填一种即可);
(2)检验Fe3+是否沉淀完全的实验操作是:取少量上层清液,滴加KSCN溶液,若不出现血红色,表明Fe(OH)3沉淀完全;
(3)酸化操作是加入盐酸,调节溶液的pH,其目的是将溶液中的少量Ca(OH)2转化为CaCl2,防止产物中混有Ca(OH)2杂质;
(4) ①测定样品的纯度过程中,a为配制一定体积物质的量浓度溶液的过程,需要用到的玻璃仪器:烧杯、玻璃棒、250mL容量瓶、胶头滴管;b、c为滴定过程,需要用到的玻璃仪器:锥形瓶、滴定管;故上述测定过程中,需要用到的玻璃仪器除了容量瓶、锥形瓶,还有烧杯、玻璃棒、胶头滴管、滴定管;②使用AgNO3溶液滴定样品的CaCl2·2H2O,n(Ag+)=0.050 mol/L×20.39 ×10-3L=1.0195 ×10-3mol,则25mL中含n(Cl-)=1.0195×10-3mol,250 mL中含n(Cl-)=1.0195×10-2mol,含n(CaCl2·2H2O)=5.0975×10-3mol,m(CaCl2·2H2O)=5.0975×10-3mol×147g·mol-1=0.7493g,样品CaCl2·2H2O的质量分数=![]() =99.9%;③蒸发结晶过程中,温度过高,使CaCl2·2H2O失去部分结晶水,而计算的时候仍按照没有失去结晶水的化合物质量计算,故最终测定的样品中CaCl2·2H2O的质量分数偏高。
=99.9%;③蒸发结晶过程中,温度过高,使CaCl2·2H2O失去部分结晶水,而计算的时候仍按照没有失去结晶水的化合物质量计算,故最终测定的样品中CaCl2·2H2O的质量分数偏高。

【题目】二氧化氯(ClO2)是世界卫生组织(WHO)推荐的A1级广谱、安全、高效消毒剂。以下是ClO2的两种制备方法:
方法一:2NaClO3 + 4HCl → 2ClO2↑+ Cl2↑+ 2NaCl + 2H2O
方法二:H2C2O4 + 2NaClO3 + H2SO4 → Na2SO4 + 2CO2↑ + 2ClO2↑ + 2H2O
完成下列填空:
(1)在方法一中,当有0.2 mol电子发生转移时,参与反应的还原剂为_________ mol。
(2)在方法二中,反应物H2C2O4_________(填序号)。
a.仅做氧化剂 b.既被氧化又被还原
c.发生氧化反应 d.既未被氧化也未被还原
(3)两种方法相比,___________(填写“方法一”或“方法二”)制备的ClO2更适合用于饮用水的消毒,其主要原因是______________________________________________。
(4)实验室也可用氯酸钠(NaClO3)和亚硫酸钠(Na2SO3)用硫酸酸化,加热制备二氧化氯,其化学反应方程式为 ________________________________________________。
(5)氯原子核外共有______种不同运动状态的电子,氯离子的最外层电子排布式是________。
(6)CCl4分子的空间构型为__________________,CO2的电子式是___________________。
(7)相同压强下,部分元素氯化物的熔点见表:
氯化物 | NaCl | KCl | CCl4 |
熔点/℃ | 804 | 773 | -22.92 |
试解释表中氯化物熔点差异的原因:_______________________________________________________。