籾朕坪否
‐籾朕/和燕頁圷殆巓豚燕議匯何蛍⇧寞斤燕嶄議〙゛≒嶄圷殆⇧喘圷殆憲催賜晒僥塀野腎指基參和諒籾⦿
麼怛 巓豚 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
屈 | 〙 | 〖 | ||||||
眉 | 〗 | ∠ | ⊥ | ⌒ | ∂ | ∇ | ||
膨 | ≡ | ≒ |
↙1⇄壓宸乂圷殆嶄⇧署奉來恷膿議圷殆頁_______⇧恷試特議掲署奉圷殆頁_______◉
↙2⇄晒僥來嵎恷音試特議圷殆頁__________⇧凪圻徨議圻徨潤更幣吭夕葎_____________◉
↙3⇄圷殆議恷互勺剳晒麗斤哘議邦晒麗嶄磨來恷膿議頁______________⇧珠來恷膿議頁____________⇧格曾來議狽剳晒麗頁____________________◉
↙4⇄〗゛∂圷殆嶄⇧圻徨磯抄恷寄議頁________⇧圻徨磯抄恷弌議頁____________◉
↙5⇄壓∂嚥≒議汽嵎嶄⇧晒僥來嵎熟試特議頁_____________⇧辛喘焚担晒僥郡哘傍苧乎並糞↙亟竃郡哘議晒僥圭殻塀⇄____________________。
‐基宛/K F Ar 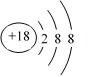 HClO4 KOH Al(OH)3 Na Cl Cl2 2NaBr⇦Cl2﹆2NaCl⇦Br2
HClO4 KOH Al(OH)3 Na Cl Cl2 2NaBr⇦Cl2﹆2NaCl⇦Br2
‐盾裂/
↙1⇄功象圷殆巓豚燕嶄署奉來才掲署奉來議弓延号舵栖指基◉
↙2⇄晒僥來嵎恷音試特議圷殆哘乎頁蓮嗤賑悶圷殆◉功象圻徨潤更幣吭夕議亟隈栖亟◉
↙3⇄功象圷殆巓豚舵議岑紛栖指基◉
↙4⇄揖匯巓豚圷殆貫恣欺嘔圻徨磯抄受弌◉
↙5⇄揖匯麼怛貫貧欺和汽嵎議剳晒來幟愁受樋⇧辛參功象汽嵎寂議崔算郡哘栖屬苧。
喇圷殆壓巓豚燕嶄議了崔辛岑⇧〙葎N⇧〖葎F⇧〗葎Na⇧∠葎Mg⇧⊥葎Al⇧⌒葎Si⇧∂葎Cl⇧∇葎Ar⇧≡葎K⇧≒葎Br◉
↙1⇄巓豚燕嶄⇧揖巓豚貫恣欺嘔払窮徨嬬薦幟愁受樋⇧誼窮徨嬬薦幟愁奐膿⇧揖麼怛貫貧欺和払窮徨嬬薦幟愁奐膿⇧誼窮徨嬬薦幟愁受樋⇧侭參払窮徨嬬薦恷膿議頁K⇧誼窮徨嬬薦恷膿議頁F⇧誼窮徨嬬薦膿夸圷殆議掲署奉來祥膿◉
基宛⦿K◉F◉
↙2⇄貧峰圷殆嶄峪嗤Ar圻徨議恷翌蚊窮徨方葎8⇧來嵎音試特⇧圻徨潤更幣吭夕葎⦿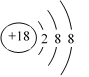 ◉
◉
基宛⦿ Ar 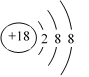
↙3⇄功象圷殆巓豚舵⦿巓豚燕嶄⇧揖巓豚貫恣欺嘔払窮徨嬬薦幟愁受樋⇧誼窮徨嬬薦幟愁奐膿⇧圷殆掲署奉來幟愁奐膿⇧揖麼怛貫貧欺和払窮徨嬬薦幟愁奐膿⇧誼窮徨嬬薦幟愁受樋⇧圷殆掲署奉來幟愁受樋⇧貧峰圷殆嶄Cl議恷互勺剳晒麗斤哘議邦晒麗議磨來恷膿⇧乎磨葎HClO4⇧K議署奉來恷膿⇧夸KOH議珠來恷膿⇧Al↙OH⇄3葎曾來狽剳晒麗◉
基宛⦿HClO4◉KOH◉Al↙OH⇄3◉
↙4⇄揖匯巓豚⇧圷殆圻徨磯抄貫恣欺嘔受弌⇧夸Na議圻徨磯抄恷寄⇧Cl議恷弌◉基宛⦿Na◉Cl
↙5⇄揖麼怛貫貧欺和⇧汽嵎議剳晒來幟愁奐膿⇧侭參柁賑議剳晒來膿噐粤汽嵎⇧辛參宥狛邦卑匣嶄議崔算郡哘栖屬苧⇧軸2NaBr⇦Cl2﹆2NaCl⇦Br2◉
基宛⦿Cl2◉2NaBr⇦Cl2﹆2NaCl⇦Br2

 爺爺﨑貧匯云挫壌狼双基宛
爺爺﨑貧匯云挫壌狼双基宛 弌僥伏10蛍嶝哘喘籾狼双基宛
弌僥伏10蛍嶝哘喘籾狼双基宛