题目内容
【题目】对复杂的有机物结构可用“键线式”表示。如苯丙烯酸1—丙烯酯: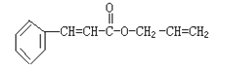 可简化为
可简化为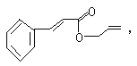 杀虫剂“阿乐丹”的结构表示为
杀虫剂“阿乐丹”的结构表示为 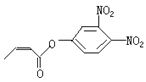 ,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
,若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是( )
A.遇FeCl3溶液均显紫色B.均能发生银镜反应
C.均能与溴水发生反应D.均能与NaOH溶液发生反应
【答案】CD
【解析】
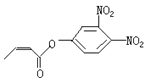 中含有酯基,可发生水解反应,水解产物为CH3CH=CHCOOH和
中含有酯基,可发生水解反应,水解产物为CH3CH=CHCOOH和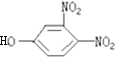 ,结合官能团的结构和性质分析解答。
,结合官能团的结构和性质分析解答。
 的水解产物为CH3CH=CHCOOH和
的水解产物为CH3CH=CHCOOH和 。
。
A.只有 含酚羟基,遇FeCl3溶液显紫色,故A错误;
含酚羟基,遇FeCl3溶液显紫色,故A错误;
B.都不含-CHO,都不能发生银镜反应,故B错误;
C.CH3CH=CHCOOH含有碳碳双键,可与溴水发生加成反应, 含有酚羟基,可与溴水发生取代反应,故C正确;
含有酚羟基,可与溴水发生取代反应,故C正确;
D.CH3CH=CHCOOH中含有羧基, 含有酚羟基,都可与氢氧化钠发生中和反应,故D正确;
含有酚羟基,都可与氢氧化钠发生中和反应,故D正确;
故选CD。

【题目】为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。

实验操作 | 实验现象 |
i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
iii.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(1)C中产生的白色沉淀是______。
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,对实验进行了改进:
打开弹簧夹,通入N2,待排净装置内空气后,关闭弹簧夹,再打开A中分液漏斗活塞,此操作的目的是_________________
②丙同学进行了进一步的改进:
在B和C之间增加盛放CCl4的洗气瓶D,丙同学的目的是______
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:
氧化性H2O2>SO2。试写出两者反应的化学方程式________________
(3)iii中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br-
观点2:B中有未反应H2SO3(或SO2)
为验证观点2,应进行的实验操作及现象是______。
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是______。