题目内容
【题目】I.2016年,我国研制的大型运输机运-20正式进入投产,标志着我国成为少数几个能生产大型军用运输机的国家之一。
(1)运-20的外壳大量使用了AM系列Mg-Al-Mn,铝的价电子排布图为_________________,第一电离能铝___________(填“大于”、“等于”或“小于”)镁
(2)为了减轻飞机的起飞重量并保持机身强度,运-20使用了大量的树脂材料,其中一种树脂材料的部分结构如图1所示,其中碳原子的杂化方式为___________,其个数比为___________


II.大型飞机的高推重比发动机被誉为航空工业皇冠上的“宝石”,采用大量的金属钨作为耐高温耐磨损材料
(3)钨元素位于第六周期第VIB族,价电子排布的能级与Cr相同,但排布方式与Cr有所不同,请写出钨原子的价层电子排布式___________
(4)图2为碳和钨形成的一种化合物的晶胞模型,碳原子和钨原子个数比为___________,其中一个钨原子周围距离最近且相等的碳原子有___________个。
【答案】 小于 sp2 、sp3 3:1 5d46s2 1:1 6
小于 sp2 、sp3 3:1 5d46s2 1:1 6
【解析】
(1)根据基态Al原子的核外电子排布式为1s22s22p63s23p1,确定铝原子的价电子排布图;镁、铝在元素周期表中位于同一周期,镁属于第ⅡA族元素,铝属于第ⅢA族元素,基态第ⅡA族元素的原子最外层电子填充的ns处于全充满,np处于全空,体系比较稳定,故基态第ⅡA族元素的原子的第一电离能比同周期相邻主族元素的第一电离能大;
(2)结合该物质的结构简式,根据价层电子对数确定该物质中碳原子的杂化方式;
(3)钨元素位于第六周期第VIB族,价电子排布的能级与Cr相同,但排布方式与Cr有所不同,根据铬原子的价层电子排布式确定钨原子的价层电子排布式;
(4)根据晶胞结构图,在顶点的原子被6个晶胞共用,在面心的原子被2个晶胞共用,在棱上的原子被3个晶胞共用,在体心的原子,不被其他晶胞共用,用于均摊法计算出晶胞中碳原子和钨原子个数。
(1)基态Al原子的价电子排布式为3s23p1,故铝的价电子排布图为 ;基态Mg原子的核外电子排布式为1s22s22p63s2, Mg元素的3s能级为全满状态,3p能级为全空状态,体系比较稳定,能量低不容易失去一个电子,所以铝的第一电离能比镁低。
;基态Mg原子的核外电子排布式为1s22s22p63s2, Mg元素的3s能级为全满状态,3p能级为全空状态,体系比较稳定,能量低不容易失去一个电子,所以铝的第一电离能比镁低。
(2)根据该树脂的结构简式,分子中的碳原子没有孤电子对,苯环中的每个碳原子形成3个![]() 键,不是苯环上的碳原子,每个碳原子形成4个
键,不是苯环上的碳原子,每个碳原子形成4个![]() 键, 所以该物质中苯环上的碳原子采用sp2杂化,不是苯环上的碳原子采用sp3杂化;采用sp2杂化的碳原子数为6n+6m,采用sp3杂化碳原子数为2m+2n,故采用sp2杂化的碳原子数与sp3杂化碳原子数之比为:(6n+6m):(2m+2n)=3:1;
键, 所以该物质中苯环上的碳原子采用sp2杂化,不是苯环上的碳原子采用sp3杂化;采用sp2杂化的碳原子数为6n+6m,采用sp3杂化碳原子数为2m+2n,故采用sp2杂化的碳原子数与sp3杂化碳原子数之比为:(6n+6m):(2m+2n)=3:1;
(3)钨元素位于第六周期第VIB族,价电子排布的能级与Cr相同,但排布方式与Cr有所不同,铬原子的价层电子排布式为3d54s1,故钨原子的价层电子排布式5d46s2;
(4)碳和钨形成的一种化合物的晶胞模型,在此结构中钨原子数目为1+2×![]() +12×
+12×![]() +6×
+6×![]() =6,晶胞内部有6个C原子,故碳原子和钨原子个数比为6:6=1:1;以晶胞体内钨原子可知,1个钨原子周围距离钨原子最近的碳原子有6个。
=6,晶胞内部有6个C原子,故碳原子和钨原子个数比为6:6=1:1;以晶胞体内钨原子可知,1个钨原子周围距离钨原子最近的碳原子有6个。
【点晴】
本题考查元素原子结构与性质相互关系的综合应用。需要注意的是,同周期中,元素原子的第一电离能的反常现象,即IIA族、VA族元素原子的价电子排布分别为ns2、ns2np3,其结构分别满足为全满和半满状态,这两族元素原子较为稳定,故第一电离能反常。如本题第(1)小题,Mg元素与Al元素第一电离能比较中,Mg>Al,因Mg原子最外层的电子3s能级处于全充满状态,3p能级处于全空状态,体系比较稳定。
![]()

 阅读快车系列答案
阅读快车系列答案【题目】实验室制备1,2-二溴乙烷的反应原理如下所示:
第一步:CH3CH2OH![]() CH2=CH2+H2O;
CH2=CH2+H2O;
第二步:乙烯与溴水反应得到1,2-二溴乙烷。
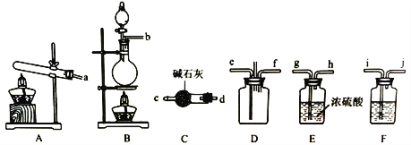
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃下脱水生成乙醚(CH3CH2OCH2CH3)。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示(部分装置未画出):

有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/(g/cm3) | 0.79 | 2.2 | 0.71 |
沸点/(℃) | 78.5 | 132 | 34.6 |
熔点/(℃) | -130 | 9 | -116 |
请回答下列问题:
(1)写出乙烯与溴水反应的化学方程式:______。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____(填字母代号)。
a.引发反应 b.加快反应速率
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是______。
(4)在装置C中应加入____ (填字母代号),其目的是吸收反应中可能生成的SO2、CO2气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___ (填“上”或“下”)层。
(6)若产物中有少量副产物乙醚,可用____的方法除去。