题目内容
【题目】已知![]() 摩尔盐
摩尔盐![]() 在
在![]() 时分解生成
时分解生成![]() 、
、![]() 和
和![]() 等。某小组称取mg样品进行如下实验
等。某小组称取mg样品进行如下实验![]() 尾气处理装置省略
尾气处理装置省略![]() ,验证它的分解产物。
,验证它的分解产物。
下列说法正确的是![]()
![]()
A.C中盐酸的作用是增强酸性,可以用硝酸替代盐酸
B.装置按![]() 连接可以检验
连接可以检验![]() 、
、![]() 、
、![]()
C.若实验中C、F都产生白色沉淀,则发生的反应不同,沉淀成分相同
D.实验完毕后,称量A中硬质玻璃管总质量,可以确定![]() 中x、y的值
中x、y的值
【答案】C
【解析】
已知![]() 摩尔盐
摩尔盐![]() 在
在![]() 时分解生成
时分解生成![]() 、
、![]() 和
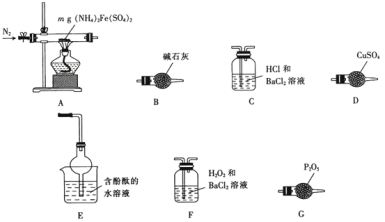
和![]() 等,装置C装置中HCl和BaCl2,可用于检验SO3;装置D用于检验H2O;装置E用于吸收和检验NH3,装置F中的H2O2和BaCl2,H2O2可氧化SO2,生成硫酸,与BaCl2反应生成白色沉淀;需要检验的产物有H2O、SOx、NH3等,检验SOx、NH3等均需要用到水溶液,因此先检验水。
等,装置C装置中HCl和BaCl2,可用于检验SO3;装置D用于检验H2O;装置E用于吸收和检验NH3,装置F中的H2O2和BaCl2,H2O2可氧化SO2,生成硫酸,与BaCl2反应生成白色沉淀;需要检验的产物有H2O、SOx、NH3等,检验SOx、NH3等均需要用到水溶液,因此先检验水。
A、装置C装置中HCl和BaCl2,可用于检验SO3,C中盐酸的作用是增强酸性,减少SO2的溶解,不可以用硝酸替代盐酸,否则硝酸会将一部分SO2氧化被BaCl2吸收,故A错误;
B、装置若按![]() 连接,
连接,![]() 经过C装置会被HCl吸收,不能在后续装置中检验到NH3,故B错误;
经过C装置会被HCl吸收,不能在后续装置中检验到NH3,故B错误;
C、若实验中C、F都产生白色沉淀,则发生的反应不同,C中发生的反应是![]() 与
与![]() 溶液反应生成硫酸钡沉淀,F中发生的反应是二氧化硫与过氧化氢发生氧化还原反应生成硫酸,硫酸与
溶液反应生成硫酸钡沉淀,F中发生的反应是二氧化硫与过氧化氢发生氧化还原反应生成硫酸,硫酸与![]() 反应生成硫酸钡沉淀,沉淀成分相同均为硫酸钡沉淀,故C正确;
反应生成硫酸钡沉淀,沉淀成分相同均为硫酸钡沉淀,故C正确;
D、实验完毕后,称量A中硬质玻璃管总质量,不可以确定![]() 中x、y的值,还需要知道其他生成物的质量,故D错误;
中x、y的值,还需要知道其他生成物的质量,故D错误;
故选C。

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目