��Ŀ����
����Ŀ����ѧ�ķ�չ�����Ľ���������ˮƽ����߶��벻����ѧ�ķ�չ���ֲ��ϵĿ������졣
(1)�й�������չѸ�٣���������ʹ�õ���Ҫ�����и��������Ͻ�Ͳ����ȡ�
�ٸ�¯������������ͨ������Ҫ�õ���ԭ����________�������½�����ʯ��ԭΪ�������Ļ�ԭ����________��
�ڸ��������Ͻ𡢲���������________������ĸ����
a.����� b.������ c.����
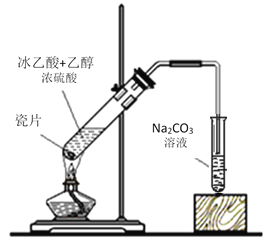
(2)������ĸ��ƣ���Ҫ������������еķ�������д�����
��ȼú�ŷŵĶ�������ᱻ��ˮ�����γ����꣬���������ڿ����о���������ǿ��ԭ����______________________________________���û�ѧ����ʽ��ʾ����
�ڵ��ʺ�����Ĺ�ҵ�����Լ������Ƚ�ͨ���ߵ�ʹ�ã����д����ĵ��������Ҫ��![]() ��
��![]() ���ŷŵ������У���Щ��������Ի�����ɵ�Ӱ����________����һ�ּ��ɣ������������������������Һ����ת��Ϊ
���ŷŵ������У���Щ��������Ի�����ɵ�Ӱ����________����һ�ּ��ɣ������������������������Һ����ת��Ϊ![]() ��________��
��________��![]() ��������װβ����ת��װ�ã��ɽ�β���еĵ��������һ����̼ת��Ϊ
��������װβ����ת��װ�ã��ɽ�β���еĵ��������һ����̼ת��Ϊ![]() ��________��
��________��
���𰸡�ʯ��ʯ����![]() ��
�� ![]() a
a ![]() �γɹ⻯ѧ����
�γɹ⻯ѧ���� ![]()
![]()
��������
(1)�ٸ�¯������ԭ��������ʯ����̿��ʯ��ʯ��������ͨ������ԭ����ʯӢɰ��ʯ��ʯ��������Ը�¯����������ͨ������Ҫ�õ���ԭ����ʯ��ʯ����������¯�У���������һ����̼��Ӧ�������Ͷ�����̼��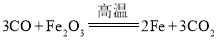 �����Խ�����ʯ��ԭ�������ʵĻ�ԭ����
�����Խ�����ʯ��ԭ�������ʵĻ�ԭ����![]() ��
��
�ڸ��������Ͻ����ںϽ����ڻ�����������Ҫ�ɷ�Ϊ�����ơ��������衢����ƣ����߶����ڻ�����ѡa��
(2)��![]() ��������ˮ������
��������ˮ������![]() ��
��![]() ����ˮ���£��������е������������������
����ˮ���£��������е������������������![]() ����
����![]() ���Ӷ�ʹ��ˮ��������ǿ��
���Ӷ�ʹ��ˮ��������ǿ��
�ڴ����ĵ��������ŷŵ������У����γɹ⻯ѧ���������������������������Һ���գ���ӦΪ![]() ��
��![]() ��������װβ����ת��װ�ã�������Ӧ
��������װβ����ת��װ�ã�������Ӧ ��
��

 A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д� ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д�����Ŀ����.��Ҫ��ش��������⣺
(1)��CO2��NH3Ϊԭ�Ϻϳ�����������CO2�ijɹ������������غϳ����е���Ҫ��Ӧ�ɱ�ʾ���£�
��Ӧ��2NH3(g)+CO2(g)![]() NH2COONH4(s)��H1
NH2COONH4(s)��H1
��Ӧ��NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g)��H2=+72.49kJ/mol
CO(NH2)2(s)+H2O(g)��H2=+72.49kJ/mol
�ܷ�Ӧ��2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)��H3=-86.98kJ/mol
CO(NH2)2(s)+H2O(g)��H3=-86.98kJ/mol
�ٷ�Ӧ�����H1=__��
��һ���¶��£�������̶����ܱ������а�n(NH3)��n(CO2)=2��1���з�Ӧ��������˵����Ӧ��ﵽ��ƽ��״̬����__������ţ���
A.������������ѹǿ���ٱ仯
B.NH3��CO2��ת�������
C.�����ڻ��������ܶȲ��ٱ仯
(2)��һ��������ܱ������н������»�ѧ��Ӧ��CO2(g)��H2(g)![]() CO(g)��H2O(g)���仯ѧƽ�ⳣ��(K)���¶�(t)�Ĺ�ϵ���±���ʾ��
CO(g)��H2O(g)���仯ѧƽ�ⳣ��(K)���¶�(t)�Ĺ�ϵ���±���ʾ��
t/�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
�ٸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=__��
�ڸ÷�ӦΪ__��������������������������Ӧ��
��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c(CO2)��c(H2)=c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ__�档
����800��ʱ������������Ӧ��ijһʱ�̲�������ڸ����ʵ�Ũ�ȷֱ�Ϊc(CO2)Ϊ2mol��L-1��c(H2)Ϊ1.5mol��L-1��c(CO)Ϊ1mol��L-1��c(H2O)Ϊ3mol��L-1����ʱ��Ӧ��__���������������������������С�
(3)��ҵ�ϴӷ�Ǧ���ط�Һ����Ǧ�Ĺ����У����ô�����Һ�봦�����Ǧ��(��Ҫ��PbSO4)������Ӧ��PbSO4(s)��CO![]() (aq)
(aq)![]() PbCO3(s)��SO
PbCO3(s)��SO![]() ( aq)��
( aq)��
��֪�ܶȻ�������Ksp(PbSO4)=1.6��10-8��Ksp(PbCO3)=7.4��10-14����÷�Ӧ�Ļ�ѧƽ�ⳣ��K=__��
��.N2H4��O2ȼ�ϵ����һ�ָ�Ч����Ⱦ�����͵�أ���װ����ͼ��ʾ��
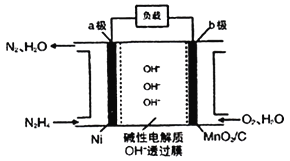
(1)N2H4�ĵ���ʽΪ__��
(2)a���ĵ缫��Ӧ����ʽΪ___��