题目内容
已知空气-锌电池的电极反应:
锌片:Zn-2OH--2e-=ZnO+H2O,
石墨:1/2O2+H2O+2e-=2OH-
据此推断锌片是( )
| A.负极,被氧化 | B.负极,被还原 |
| C.正极,被氧化 | D.正极,被还原 |
A
解析

练习册系列答案
 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案
相关题目
观察下列几个装置示意图,有关叙述错误的是( )
| A.装置①中烧杯内中加入黄色的K3[Fe(CN)6]溶液,一段时间后看不到Fe电极附近有蓝色沉淀生成,该装置可看作金属的析氢腐蚀 |
| B.装置②盐桥中的Cl—向硫酸铜溶液移动 |
| C.装置③中外电路电流方向:b极 →a极 |
| D.装置④中阳极反应:2 Cl——2e- = Cl2 ↑ |
下列图示的有关说法正确的是
| A.装置①中负极反应式为H2+2e一=2H+ |
| B.装置①工作时,外电路电子由a电极流向b电极 |
| C.若采用装置②精炼铜,则d为粗铜,c为纯铜 |
| D.若装置②用惰性电极电解稀H2SO4溶液,则溶液pH升高 |
某小组为研究电化学原理,设计如图装置。下列叙述不正确的是 ( )
| A.a和b分别与电源的负极正极相连时,电解氯化钠溶液产生氯气 |
| B.a和b用导线连接时,碳棒上发生的反应为:O2+2H2O+4e-=4OH- |
| C.若往溶液中加少许硫酸,无论a和b是否连接,铁片均会溶解,溶液逐渐变成浅绿色 |
| D.若氯化钠溶液改为氯化铵溶液,a和b连接,碳棒上有气泡产生 |
下列关于原电池的叙述中正确的是( )。
| A.正极和负极必须是两种不同的金属 |
| B.电子流入的一极为正极 |
| C.原电池工作时,正极和负极上发生的都是氧化还原反应 |
| D.锌、铜和盐酸构成的原电池工作时,锌片上有6.5 g锌溶解,正极上就有0.1 g氢气生成 |
锌、稀硫酸和铜组成的原电池装置中,当导线中有1 mol电子通过时,理论上两极的变化是( )
①锌片溶解32.5g;②锌片增重32.5g;
③铜片上析出1g H2;④铜片上析出1mol H2
| A.①和③ | B.①和④ | C.②和③ | D.②和④ |
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳。其中一种镁电池的反应为xMg+Mo3S4 MgxMo3S4,下列说法错误的是( )
MgxMo3S4,下列说法错误的是( )
| A.放电时Mg2+向正极迁移 |
| B.放电时正极反应为Mo3S4+2xe-=Mo3S42x- |
| C.充电时Mo3S4发生氧化反应 |
| D.充电时阴极反应为Mg2++2e-=Mg |
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池说法正确的是( )
| A.在熔融电解质中,O2-由负极移向正极 |
| B.通入空气的一极是正极,电极反应为:O2+2H2O+4e-=4OH- |
| C.通入丁烷的一极是负极,电极反应为:C4H10+26e-+13O2-=4CO2+5H2O |
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体为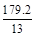 L L |
