题目内容
【题目】下列离子方程式中,属于水解反应的是( )
A. HCOOH+H2O![]() HCOO— + H3O+ B. CO2+H2O
HCOO— + H3O+ B. CO2+H2O![]() HCO3— + H+
HCO3— + H+
C. SO32— + H2O![]() HSO3— + OH— D. HS— + H2O
HSO3— + OH— D. HS— + H2O![]() S2— + H3O+
S2— + H3O+
【答案】C
【解析】HCOOH+H2O![]() HCOO— + H3O+即可改为HCOOH
HCOO— + H3O+即可改为HCOOH ![]() HCOO— + H+,属于甲酸的电离方程式,A项不符合题意;CO2+H2O
HCOO— + H+,属于甲酸的电离方程式,A项不符合题意;CO2+H2O![]() H2CO3
H2CO3![]() HCO3— + H+属于碳酸的电离方程式,B项不符合题意;SO32— + H2O
HCO3— + H+属于碳酸的电离方程式,B项不符合题意;SO32— + H2O![]() HSO3— + OH—属于亚硫酸的水解反应方程式,C项符合题意;HS— + H2O
HSO3— + OH—属于亚硫酸的水解反应方程式,C项符合题意;HS— + H2O![]() S2— + H3O+即可改为HS—
S2— + H3O+即可改为HS— ![]() S2— + H+,属于HS—的电离方程式,D项不符合题意。
S2— + H+,属于HS—的电离方程式,D项不符合题意。

【题目】用氮化硅陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g)![]() Si3N4(s)+12HCl(g)在温度T0下的2L密闭容器中,加入0.30mol SiCl4 , 0.20mol N2.0.36mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80g
Si3N4(s)+12HCl(g)在温度T0下的2L密闭容器中,加入0.30mol SiCl4 , 0.20mol N2.0.36mol H2进行上述反应,2min后达到平衡,测得固体的质量增加了2.80g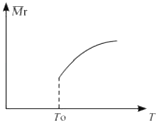
(1)SiCl4的平均反应速率为
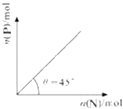
(2)平衡后,若改变温度,混合气体的平均相对分子质量与温度的关系如图所示,下列说法正确的是( )
A.该反应在任何温度下可自发进行
B.若混合气体的总质量不变,表明上述反应己达到平衡状态
C.其他条件不变,增大Si3N4的物质的量,平衡向左移动
D.按3:2:6的物质的量比增加反应物,SiCl4(g)的转化率降低
(3)下表为不同温度下该反应的平衡常数,其他条件相同时,在(填“T1”、“T2”、“T3”)温度下反应达到平衡所需时间最长:
温度T | T1 | T2 | T3 |
平衡常数K | 1.2 | 2.5 | 10 |
假设温度为T1时向该反应容器中同时加入.c(SiCl4)=0.3mol/L,c(H2)=0.3mol/L,c(N2)=x mol/L,c(HCl)=0.3mol/L和足量Si3N4 (s),若要使平衡建立的过程中HCl浓度减小,x的取值范围为
(4)该反应的原子利用率为
(5)工业上制备SiCl4的反应过程如下:
①SiO2(s)+2C(s)═Si(s)+2CO(g),△H═akJ/mol
②Si(s)+2Cl2(g)═SiCl4(l),△H=bkJ/mol
③SiCl4(g)═SiCl4(l),△H═ckJ/mol
写出二氧化硅、焦炭与Cl 2在高温下反应生成气态SiCl4和一氧化碳的热化学方程式 .