题目内容
17.某地污水中含有Zn2+、Hg2+、Fe3+、Cu2+四种阳离子.甲、乙、丙三位同学设计的从该污水中回收金属铜的方案如下:甲:污水$→_{①}^{+NaOH溶液,过滤}$沉淀$→_{②}^{△}$ CuO$→_{③}^{+H_{2}△}$ Cu
乙:污水$→_{①}^{+过量铁粉,过滤}$滤渣$→_{②}^{△}$CuO$→_{③}^{+H_{2}△}$ Cu
丙:污水$→_{①}^{+过量铁粉,过滤}$滤渣$→_{②}^{+稀盐酸,过滤}$滤渣$→_{③}^{△}$CuO$→_{④}^{+H_{2},△}$Cu
下列判断正确的是( )
| A. | 三种实验方案都能制得纯净的铜 | |
| B. | 乙方案中加过量铁粉可以将四种阳离子全部还原 | |
| C. | 甲方案中的反应涉及置换、分解、化合、复分解四种反应类型 | |
| D. | 丙方案会产生环境污染 |
分析 甲中生成沉淀含氢氧化铜、氢氧化铁,不利用制备纯Cu;乙中滤渣含Fe、Cu,不利于制备纯铜,丙中加铁粉后的滤渣含Fe、Cu,再加盐酸除去Fe,得到的滤渣只有Cu,以此来解答.
解答 解:甲中生成沉淀含氢氧化铜、氢氧化铁,不利用制备纯Cu;乙中滤渣含Fe、Cu,不利于制备纯铜,丙中加铁粉后的滤渣含Fe、Cu,再加盐酸除去Fe,得到的滤渣只有Cu,A.由上述分析可知,只有丙可制备纯Cu,故A错误;
B.乙方案中加过量铁粉可以将Fe3+、Hg2+和Cu2+全部还原,故B错误;
C.甲方案中的反应涉及③为置换、②为分解、①为复分解三种反应类型,故C错误;
D.由上述分析可知,丙方案回收铜较好,但有盐酸废液,发生环境污染,故D正确.
故选D.
点评 本题考查物质的分离提纯方法及选择,为高频考点,把握物质的性质及制备流程中的反应为解答的关键,注意发生的反应的分析及物质的成分,题目难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
13.已知,淀粉制酒精的反应分别为:(C6H10O5)n (淀粉)+nH2O $\stackrel{催化剂}{→}$nC6H10O6 (葡萄糖)、C6H10O6 $\stackrel{催化剂}{→}$2CH3CH2OH+2CO2 ↑.某厂欲用2t的含淀粉54%的薯干制酒精,如果在发酵过程中有85%的淀粉转化为乙醇.且制得的酒精中含5%的水,则可制得这样的酒精( )
| A. | 0.85t | B. | 0.65t | C. | 1.55t | D. | 0.55t |
5.下列各组物质形成的晶体中,晶体类型相同的是( )
| A. | 晶体硅和SiC | B. | C60和Mg | C. | NaCl和HCl | D. | SO2和SiO2 |
12.由Li、Al、Si构成的某三元化合物固态晶体结构如图所示,下列说法正确的是( )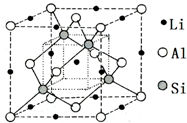

| A. | 该化合物化学式可表示为LiAlSi | |
| B. | 晶体中Al和Li构成CsCl型骨架 | |
| C. | 晶体中Al和Si构成金刚石型骨架 | |
| D. | 晶体中与每个Al距离最近的Li为4个 |
2.下列烃和H2加成反应可生成3-甲基己烷的是( )
| A. | CH2=CHCH(CH3)CH2CH2CH2CH3 | B. | CH2=CHC(CH3)=CHCH2CH3 | ||
| C. | CH2=CHCH(CH3)C≡CH | D. | CH3CH2CH2CH2C(CH3)=CH2 |
9.下列烷烃的系统命名中,不正确的是( )
| A. | 2,3-二甲基戊烷 | B. | 3-甲基-2-乙基己烷 | ||
| C. | 3,3-二甲基戊烷 | D. | 3-甲基-1-丁烯 |
6.下列说法正确的是( )
| A. | 两种化合物组成元素相同,且各元素的质量分数也相同,则两者一定是同分异构体 | |
| B. | 分子中有6个碳原子的烃只能形成5个碳碳单键 | |
| C. | 丙烯分子中的所有原子都在同一平面内 | |
| D. | 分子式为C3H6Cl2与C3H2Cl6的有机物所具有的同分异构体数目相同 |
7.据碘与氢气反应的热化学方程式
(1)I2(g)+H2(g)?2HI(g)△H=-9.48 kJ•mol-1
(2)I2(s)+H2(g)?2HI(g)△H=+26.48 kJ•mol-1
下列判断正确的是( )
(1)I2(g)+H2(g)?2HI(g)△H=-9.48 kJ•mol-1
(2)I2(s)+H2(g)?2HI(g)△H=+26.48 kJ•mol-1
下列判断正确的是( )
| A. | 254gI2( g)中通入 2gH2( g),反应放热 9.48 kJ | |
| B. | 1mol固态碘与1mol气态碘所含的能量相差17.00kJ | |
| C. | 反应(1)的产物比反应(2)的产物稳定 | |
| D. | 反应(2)的反应物总能量比反应(1)的反应物总能量低 |