题目内容
4.在强酸性溶液中能大量共存的离子组是( )| A. | K+、Na+、NO3-、CO32- | B. | K+、Na+、Br-、SO32- | ||
| C. | K+、Na+、I-、SO42- | D. | Na+、K+、CH3COO-、SO42- |
分析 强酸性溶液中存在大量氢离子,
A.碳酸根离子与氢离子反应;
B.亚硫酸根离子与氢离子反应;
C.四种离子之间不反应,都不与氢离子反应;
D.醋酸根离子与氢离子反应生成弱电解质醋酸.
解答 解:A.CO32-与强酸性溶液中的氢离子反应,在溶液中不能大量共存,故A错误;
B.SO32-与酸性溶液中的氢离子反应,在溶液中不能大量共存,故B错误;
C.K+、Na+、I-、SO42-之间不发生反应,都不与氢离子反应,在溶液中能够大量共存,故C正确;
D.CH3COO-与酸性溶液中的氢离子反应生成醋酸,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的正误判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
15.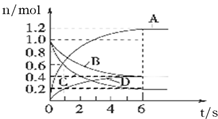 一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )
 一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体,发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断不合理的是( )| A. | 该反应的化学方程式为3B+4C═6A+2D | |
| B. | 反应进行到1s时,v(A)和v(D)不相等 | |
| C. | 反应开始到6s,B的平均反应速率为0.1mol•L-1•s-1 | |
| D. | 反应进行到6s时,各物质的浓度不再变化,达到平衡状态 |
12.完全燃烧1g氢气,生成液态的水,释放出143KJ的热量,下列热化学方程式描述正确的是( )
| A. | H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-143kJ•mol-1 | B. | 2H2(g)+O2(g)═2H2O(g)△H=-286 kJ•mol-1 | ||
| C. | 2H2O(l)═2H2(g)+O2(g)△H=+286 kJ•mol-1 | D. | H2O(l)═H2(g)+$\frac{1}{2}$O2(g)△H=+286 kJ•mol-1 |
19.FeCl3溶液与下列物质的反应,其中与Fe3+的水解无关的一组是( )
①紫色石蕊试液
②碘化钾
③煮沸的蒸馏水
④硫化氢
⑤苯酚
⑥铜粉
⑦小苏打溶液
⑧镁粉.
①紫色石蕊试液
②碘化钾
③煮沸的蒸馏水
④硫化氢
⑤苯酚
⑥铜粉
⑦小苏打溶液
⑧镁粉.
| A. | ②④⑤⑥ | B. | ①②④ | C. | ③⑧ | D. | ②④⑧ |
9.在探究新制饱和氯水成分的实验中,下列根据实验现象与结论不正确的是( )
| A. | 氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 | |
| B. | 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- | |
| C. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ | |
| D. | 向紫色石蕊试液中滴加氯水,溶液最终变成白色,说明氯水中含有HClO |
16.能用H++OH-=H2O来表示的化学反应是( )
| A. | Ba(OH)2溶液滴入稀硫酸中 | B. | 氢氧化钠溶液和稀硝酸反应 | ||
| C. | 氢氧化镁和稀盐酸反应 | D. | NaOH溶液滴入醋酸中 |
13.家用炒菜锅用水清洗后,出现红棕色的锈斑.此变化过程不发生的化学反应是( )
| A. | 4Fe(OH)2+2H2O+O2═4Fe(OH)3 | B. | 2Fe+2H2O+O2═2Fe(OH)2 | ||
| C. | 负极反应:Fe-3e-═Fe3+ | D. | 正极反应:2H2O+O2+4e--═4OH- |
14.根据如图海水综合利用的工业流程图,判断下列说法正确的是( )
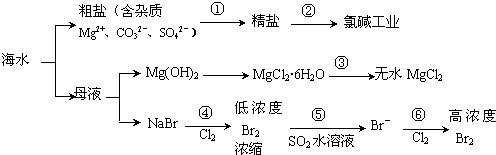

| A. | 过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 | |
| B. | 除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 | |
| C. | 在过程③中将MgCl2•6H2O灼烧即可制得无水MgCl2 | |
| D. | 在过程④、⑥反应中每氧化0.2 mol Br-需消耗0.1mol Cl2 |
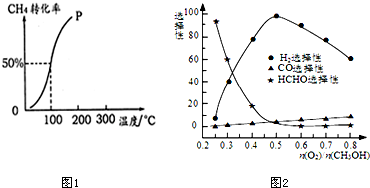 甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.工业生产甲醇的常用方法是:CO(g)+2H2(g)?CH3OH(g)△H=-90.8 kJ•mol-1
甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.工业生产甲醇的常用方法是:CO(g)+2H2(g)?CH3OH(g)△H=-90.8 kJ•mol-1