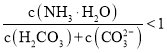题目内容
【题目】下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
A.在0.1molL-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
B.在0.1molL-1Na2CO3溶液中:c(OH-)+c(H+)=c(HCO3-)+2c(H2CO3)
C.向0.2molL-1NaHCO3溶液中加入等体积0.1molL-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
D.常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1molL-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
【答案】D
【解析】
根据盐类的水解规律进行分析;根据物料守恒、质子守恒、电荷守恒规律进行解答。
A.碳酸氢钠溶液中,碳酸氢根离子的电离程度小于其水解程度,溶液显示碱性,则:![]() ,溶液中正确的粒子难度大小为:
,溶液中正确的粒子难度大小为:![]() ,故A错误;
,故A错误;
B.根据碳酸钠溶液中的质子守恒可得:![]() ,故B错误;
,故B错误;
C.向![]() 溶液中加入等体积
溶液中加入等体积![]() 溶液,反应后溶质为等浓度的
溶液,反应后溶质为等浓度的![]() 、
、![]() ,
,![]() 的水解程度大于
的水解程度大于![]() ,则:
,则:![]() ,溶液中正确的离子浓度关系为:
,溶液中正确的离子浓度关系为:![]() ,故C错误;
,故C错误;
D.![]() 和
和![]() 混合溶液的
混合溶液的![]() ,则
,则![]() ,根据电荷守恒可得:c(Na+) = c(CH3COO-) = 0.1 mol/L,溶液中离子浓度大小为:
,根据电荷守恒可得:c(Na+) = c(CH3COO-) = 0.1 mol/L,溶液中离子浓度大小为:![]() ,故D正确;
,故D正确;
答案:D。

练习册系列答案
 同步奥数系列答案
同步奥数系列答案
相关题目