��Ŀ����
11��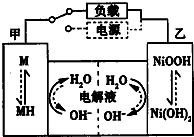 �������ٻ��š����ֵ÷з�����ķ���Prius���ڵ�������϶������������õ綯������ȼ������߽���������֣��������»����ʱ���綯���ṩ�ƶ��������������͵����ģ���ɲ��������ʱ�綯�����ڳ��״̬��
�������ٻ��š����ֵ÷з�����ķ���Prius���ڵ�������϶������������õ綯������ȼ������߽���������֣��������»����ʱ���綯���ṩ�ƶ��������������͵����ģ���ɲ��������ʱ�綯�����ڳ��״̬����1����϶���������ȼ��������Ϊȼ�ϣ����ͣ�������C8H18�ƣ���������ַ�Ӧ��ÿ����1molˮ�����ͷ���569.1kJ����÷�Ӧ���Ȼ�ѧ����ʽΪC8H18��l��+$\frac{25}{2}$O2��g��=8CO2��g��+9H2O��g������H=-5121.9kJ•mol-1��
��2����϶������ĵ綯��Ŀǰһ��ʹ�õ�������أ������ز������Ļ�����Ϊ�����������������M��ʾ��Ϊ��������Һ����ҪΪKOH��Ϊ���Һ�������س�ŵ�ԭ��ʾ����ͼ�����ܷ�Ӧʽ�ǣ�H2+2NiOOH$?_{�ŵ�}^{���}$2Ni��OH��2������������Ϣ�жϣ���϶��������»�ɲ��ʱ���缫��Χ��Һ��pH����������������䡱��С�������ҵ缫�ĵ缫��ӦʽΪNi��OH��2+OH--e-=NiOOH+H2O��
��3�����ø����������ö��Ե缫�������ͭ��Һ��һ��ʱ���ȡ���缫����������Һ�м���9.8gCu��OH��2����ַ�Ӧ��������Һ����ǰ��ͬ�����������ı�״����H2�����Ϊ4.48L��
���� ��1���������ʵ�״̬����Ӧ�е������仯�����ʵ����뷴Ӧ�ȵĹ�ϵ����д�Ȼ�ѧ����ʽ��
��2����ɲ��������ʱ��ش��ڳ��״̬�����صĹ���ԭ�����缫�������������ӷ����õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H2O+2e-=H2��+2OH-���ҵ缫Ϊ����������������ת��ΪNiOOH�Ĺ��̣���ӦʽΪNi��OH��2+OH--e-=NiOOH+H2O��
��3�����ݵ��صĹ���ԭ����Ҫ���õ���ĵ���ʸ�ԭ������ѭ��ԭ���ǣ���ʲô��ʲô������ Cu��OH��2����Һ����ǰ��ͬ����ͭ���Ӻ��������ŵ磬���ݵ����غ���㣮
��� �⣺��1������ȼ������1molˮ��������569.1kJ����������9molˮ��������5121.9kJ����������ȼ�յ��Ȼ�ѧ��Ӧ����ʽΪC8H18��l��+$\frac{25}{2}$O2��g��=8CO2 ��g��+9H2O��g������H=-5121.9kJ•mol-1��
�ʴ�Ϊ��C8H18��l��+$\frac{25}{2}$O2��g��=8CO2 ��g��+9H2O��g������H=-5121.9kJ•mol-1��
��2����ɲ��������ʱ��ش��ڳ��״̬�����صĹ���ԭ�����缫�������������ӷ����õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H2O+2e-=H2��+2OH-�����Լ缫��Χ��Һ��pH�������ҵ缫Ϊ����������������ת��ΪNiOOH�Ĺ��̣���ӦʽΪNi��OH��2+OH--e-=NiOOH+H2O��
�ʴ�Ϊ������Ni��OH��2+OH--e-=NiOOH+H2O��
��3���Զ��Ե缫���CuSO4��Һ�ĵ��ԭ������ʽ�ǣ�2Cu2++2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+4H++O2��������9.8g Cu��OH��2���൱��CuO��H2O������Һ����ǰ��ͬ������ͭԪ���غ㣬������������ͭ�����ʵ�����0.1mol��������Ӧ�ǣ�2Cu2++4e-��2Cu������������ͭ�����ʵ�����0.1molʱ����ת�Ƶĵ�����0.2mol��������0.1molˮʱ��ת�Ƶ�����0.2mol���ܹ�ת�Ƶ�����0.4mol��������1mol����ת��2mol���ӣ�����ת�Ƶ�����0.4mol�����ĵ��������Ϊ$\frac{1}{2}$��0.4��22.4=4.48L��
�ʴ�Ϊ��4.48��
���� ���⿼����ԭ���ԭ�����Ȼ�ѧ��Ӧ����ʽ����д���ѶȲ���ע���Ȼ�ѧ��Ӧ����ʽ�з�Ӧ����������Ĺ�ϵ���������ı䣬��Ӧ��Ҫ��Ӧ�ĸı��Լ�ע������غ�˼���Ӧ�ã�

| A�� | ����c��X����X��ת�������� | B�� | �����¶ȣ�Y��ת�������� | ||
| C�� | ��С���������ƽ�������ƶ� | D�� | ���������Z�IJ������� |
| A�� | NO | B�� | SO2 | C�� | CO2 | D�� | NO2 |
| A�� | �ơ����Ż�ʱ��ˮ��� | |
| B�� | ��ȼ����ǰҪ�鴿����ȼ����ǰ�����鴿 | |
| C�� | ŨNaOH��Һ����Ƥ���ϣ�������ˮ��ϴ��Ȼ��Ϳ��Ũ���� | |
| D�� | ϡ��Ũ����ʱ��Ϊ��ֹҺ��ɽ�����Ũ�������ձ��ڻ�������ˮ�У������Ͻ��� |
| A�� | 18gH2O�����ĵ�����ĿΪ9N0 | |
| B�� | 0.1 mol/L Na2SO4��Һ����Na+��ĿΪ0.2N0 | |
| C�� | 1 mol����ȫ��Ӧʱ��ʧȥ�ĵ�����ΪN0 | |
| D�� | ��״����22.4L O2������ԭ����ĿΪN0 |
����ҵ��������֪3H2��g��+CO2��g��?CH3OH��g��+H2O ��g����H=-49.5KJ/mol
H2��g��+CO2��g��?CO��g��+H2O ��g����H=+41.3KJ/mol
��1��д����H2 ��CO �� CH3OH ���Ȼ�ѧ����ʽCO��g��+2H2��g��=CH3OH��g����H=-90.8KJ/mol
��2��H2 ��CO ���Է���Ӧ����CH3OH�������ǵ���
��3��ij�¶��£�1���е�ƽ�ⳣ��Ϊ1.2����ʹƽ�ⳣ����Ϊ2������������D
A������ѹǿ B������CO��Ũ�� C�������¶� D�������¶� E��ʹ�ô���
��4����һ���¶����ܱ������У���H2��CO2�����3��1����Ͷ�ϣ�3H2+CO2?CH3OH+H2O ��Ӧ�ﵽƽ��ı�־��BC
A��ƽ�ⳣ������ B��CO2��ת���ʲ���
C����������ƽ����Է����������ٸı� D�����������ܶȲ���
���� ����ͬ���ʵ�����H2O��g���� CO�ֱ�ͨ�����Ϊ2L�ĺ����ܱ������У�������Ӧ��H2O��g��+CO��g��fCO2��g��+H2��g����H���õ��������ݣ�
| ʵ�� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| H2O | CO | CO | H2 | |||
| I | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| II | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| III | 900 | 2 | 1 | a | b | t |
��2����ƽ��ʱʵ����ʵ�����H2O��g����ת���ʵĴ�С��ϵΪ��a2��HO����a3��H2O�������������������=������
���� һ�������·�Ӧ��6H2��g��+2CO2��g��?C2H5OH ��g��+3H2O��g����H�����й�������ͼ1��ʾ��
��1������˵����ȷ����C
A�����ߢ��Ӧ�ķ�Ӧ����ʼ���ʵ���Ϊ1.5 B����ƽ��ʱ��v��H2����=v��CO2����
C��a���Ӧ��H2��ƽ��ת����Ϊ90% D��b���Ӧ��ƽ�ⳣ��Kֵ����c��
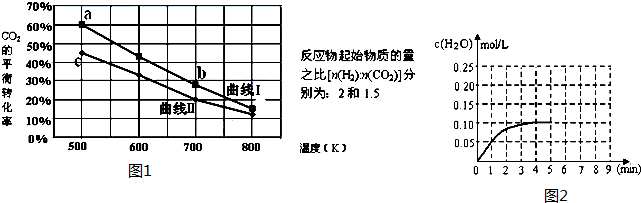
��2���¶�ΪT1ʱCO��g��+H2O��g��?H2��g��+CO2��g���������Ϊ2�����ܱ� �����м���0.4molCO2��0.4mol H2����4���Ӵﵽƽ�⣬��Ӧ��H2O��Ũ�ȱ仯�����ͼ��ʾ���ڵ�5����ʱ����ϵ���ٳ���0.2molCO2��0.2mol H2���������������䣩����8���Ӵ�ƽ�⣬����ͼ2�л���5��9���ӵ�H2O��Ũ�ȱ仯���ߣ�
| A�� | ��NaOH�����������ƿ���ܽ� | |
| B�� | �ܽ�NaOH����Һ��ȴ�����º�ת�Ƶ�����ƿ�� | |
| C�� | ���ݺ�����ƿ����ҡ�ȣ�����Һ�潵�ͣ�������ˮ���̶��� | |
| D�� | ����ʱ����Һ�棬������ҺŨ��ƫ�� |

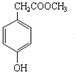 �ķ���ʽ��C9H10O3��1mol������I��ȫȼ�գ�����10mol������
�ķ���ʽ��C9H10O3��1mol������I��ȫȼ�գ�����10mol������