题目内容
20.(1)化合物Ⅰ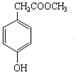 的分子式是C9H10O3,1mol化合物I完全燃烧,消耗10mol氧气.
的分子式是C9H10O3,1mol化合物I完全燃烧,消耗10mol氧气.(2)下列关于化合物I的说法,正确的是ABD.
A、化合物I可与浓溴水反应生成白色沉淀
B、1mol化合物I最多能与2mol氢氧化钠发生反应
C、化合物I可以发生银镜反应
D、化合物I的核磁共振氢谱有五个峰.
分析 (1)根据结构简式知,该物质分子式为C9H10O3;其分子式转化为C9H4(H2O)3 ,1mol该物质耗氧量=1mol×(9+$\frac{4}{4}$)mol;
(2)A、含有酚羟基,能和浓溴水发生取代反应;
B、酚羟基和酯基水解生成的羧基能和NaOH反应;
C、不含醛基,没有醛的性质;
D、化合物I中氢原子种类有5种.
解答 解:(1)根据结构简式知,该物质分子式为C9H10O3;其分子式转化为C9H4(H2O)3 ,1mol该物质耗氧量=1mol×(9+$\frac{4}{4}$)mol=10mol;
故答案为:C9H10O3;10;
(2)A、含有酚羟基,能和浓溴水发生取代反应生成白色沉淀,故A正确;
B、酚羟基和酯基水解生成的羧基能和NaOH反应,1mol化合物I最多能与2mol氢氧化钠发生反应
,故B正确;
C、不含醛基,没有醛的性质,所以不能发生银镜反应,故C错误;
D、化合物I中氢原子种类有5种,所以化合物I的核磁共振氢谱有五个峰,故D正确;
故选ABD.
点评 本题考查有机物结构和性质及根据方程式进行计算,为高频考点,明确官能团及其性质关系是解本题关键,难点是(1)中计算,会利用解题技巧解答问题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列说法正确的是( )
| A. | 室温下,CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) | |
| B. | 相同温度下,0.6 mol•L-1氨水和0.3 mol•L-1氨水中c(OH-)之比是2:1 | |
| C. | 向0.1 mol•L-1NaNO3溶液中滴加盐酸使溶液的pH=5,此时混合液中的c(Na+)=c(NO3-) | |
| D. | 室温下,0.1 mol•L-1NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):则c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) |
15.某强酸性溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下
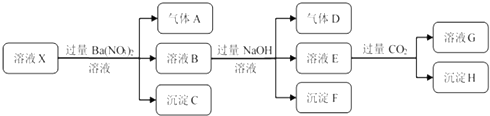
下列有关推断合理的是( )

下列有关推断合理的是( )
| A. | 若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.05 mol•L-1 | |
| B. | 沉淀H为Al(OH)3、BaCO3的混合物 | |
| C. | 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- | |
| D. | 根据上述连续实验不能确定溶液X中是否含有Fe3+ |
5.根据元素性质周期表递变规律,下列判断均正确的是( )
| A. | 酸性:HClO4>HBrO4>HIO4 碱性:NaOH>KOH>RbOH | |
| B. | 原子半径:Na>O>F 离子半径::Na+>O2->F- | |
| C. | 稳定性::HF>H2O>H2S 还原性:HCl<H2S<PH3 | |
| D. | 还原性:Na>Mg>Al 氧化性:P>S>Cl2 |
9.关于Na2CO3和NaHCO3性质的说法正确的是( )
| A. | 25℃时,在水中的溶解度NaHCO3大于Na2CO3 | |
| B. | 用Ba(OH)2溶液能鉴别碳酸钠和碳酸氢钠溶液 | |
| C. | 受热时,NaHCO3比Na2CO3容易分解 | |
| D. | NaHCO3和Na2CO3各1mol分别与过量盐酸充分反应,产生CO2的质量不同 |
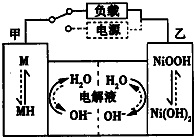 近期因“召回门”而闹得沸沸扬扬的丰田Prius属于第三代混合动力车,可以用电动机、内燃机或二者结合驱动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.
近期因“召回门”而闹得沸沸扬扬的丰田Prius属于第三代混合动力车,可以用电动机、内燃机或二者结合驱动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.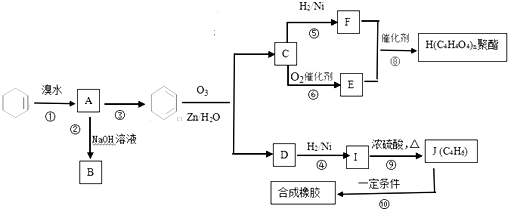
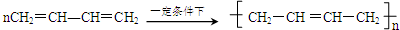 .
.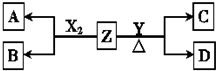 短周期元素组成的单质X2,Y.常温下,X2是一种黄绿色气体,Y为淡黄色固体,Z是一种常见的碱,焰色反应呈浅紫色(透过钴玻璃)且0.1mol•L-1 Z的水溶液pH=13.X2、Y 和Z之间有如图转化关系(其他无关物质已略去)
短周期元素组成的单质X2,Y.常温下,X2是一种黄绿色气体,Y为淡黄色固体,Z是一种常见的碱,焰色反应呈浅紫色(透过钴玻璃)且0.1mol•L-1 Z的水溶液pH=13.X2、Y 和Z之间有如图转化关系(其他无关物质已略去)