题目内容
【题目】下列各图示中不能较长时间看到Fe(OH)2白色沉淀的是
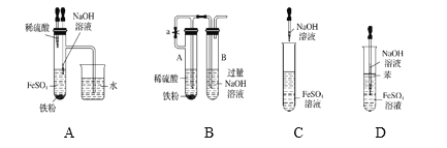
A.AB.BC.CD.D
【答案】C
【解析】
Fe(OH)2是白色不溶于水的物质,在空气中易被氧化迅速变为灰绿色,最终变为红褐色的Fe(OH)3。
A. 稀硫酸与铁粉反应生成氢气,生成的氢气将装置中的空气排出,可避免Fe(OH)2被氧化为Fe(OH)3,可长时间看到Fe(OH)2白色沉淀,不符合题意,不能选择A;
B. 铁粉与稀硫酸反应生成的氢气将装置中的空气排出,且利用氢气的压力使氢氧化钠溶液与硫酸亚铁溶液接触而发生反应,可防止Fe(OH)2被氧化为Fe(OH)3,可长时间看到Fe(OH)2白色沉淀,不符合题意,不能选择B;
C. 装置中没有隔绝空气,生成的Fe(OH)2被氧化为Fe(OH)3,不能长时间看到Fe(OH)2白色沉淀,符合题意,选择C;
D. 苯的密度小于溶液的密度,浮在上层,在一定程度上可隔绝空气,防止Fe(OH)2被氧化为Fe(OH)3,可长时间看到Fe(OH)2白色沉淀,不符合题意,不能选择D;
答案选C。

【题目】温度为T时,在三个容积均为1L的恒容密闭容器中仅发生反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,达到平衡时,下列说法不正确的是
2SO3(g) ΔH<0,达到平衡时,下列说法不正确的是
容器 编号 | 容器类型 | 起始物质的量 / mol | 平衡时SO3的物质的量 / mol | ||
SO2 | O2 | SO3 | |||
I | 恒温恒容 | 2 | 1 | 0 | 1.8 |
II | 恒温恒压 | 2 | 1 | 0 | a |
III | 绝热恒容 | 0 | 0 | 2 | b |
A. 容器I中SO2的转化率小于容器II中SO2的转化率
B. 容器II的平衡常数大于容器III中的平衡常数
C. 平衡时SO3的物质的量:a>1.8、b>1.8
D. 若起始时向容器I中充入0.10 mol SO2(g)、0.20mol O2(g)和2.0 mol SO3(g),则此时v正<v逆