题目内容
18.对一个有气体参与的反应,下列能加快反应速率且不改变活化分子百分数的是( )| A. | 定容容器中通入惰性气体 | B. | 增大压强 | ||
| C. | 升温 | D. | 加入催化剂 |
分析 升高温度或加入催化剂可提高反应物中的活化分子百分数,增大浓度、增大压强时单位体积内活化分子数目增大,活化分子百分数不变,据此进行判断.
解答 解:A、定容容器中通入惰性气体,活化分子数目不变,反应速率不变,故A错误;
B、增大压强时单位体积内活化分子数目增大,化学反应速率加快,活化分子百分数不变,故B正确;
C、升高温度可提高反应物中的活化分子百分数,故C错误;
D、加入催化剂可提高反应物中的活化分子百分数,故D错误;
故选B.
点评 本题考查影响活化分子百分数的因素,题目难度不大,注意相关知识的积累.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
20.下列叙述正确的是( )
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子 | |
| B. | 在水溶液中能离解为自由移动的离子的化合物是电解质 | |
| C. | CO2的水溶液导电能力很弱,故CO2是弱电解质 | |
| D. | 在强电解质的水溶液中只有离子没有分子 |
1.电闪雷鸣的雨天,空气中的N2会发生一系列反应,生成氮的化合物.雷雨时,一般不可能生成的氮的化合物是( )
①NH3 ②NO ③NO2 ④N2O3 ⑤N2O5 ⑥HNO3.
①NH3 ②NO ③NO2 ④N2O3 ⑤N2O5 ⑥HNO3.
| A. | ②④⑥ | B. | ②③⑤⑥ | C. | ①④⑤ | D. | ①③⑤ |
6.下列化学方程式或离子方程式正确的是( )
| A. | 乙酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O | |
| B. | 甲醛与足量新制Cu(OH)2浊液反应:HCHO+2Cu(OH)2$\stackrel{△}{→}$HCOOH+Cu2O↓+2H2O | |
| C. | 实验室用液溴和苯在催化剂作用下制溴苯: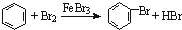 | |
| D. | 将CO2通入苯酚钠溶液: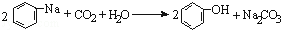 |
13.将 转变为
转变为 的方法为( )
的方法为( )
 转变为
转变为 的方法为( )
的方法为( )| A. | 与足量NaOH溶液共热后,再通入CO2 | |
| B. | 与稀H2SO4共热后,加入足量Na2CO3 | |
| C. | 与稀H2SO4共热后,加入足量NaOH | |
| D. | 与足量NaOH溶液共热后,再加入稀硫酸 |
10.甲烷燃料电池以铂为电极、KOH溶液为电解质溶液,在两极区分尉通入甲烷和氧气即可产生电流.下列叙述正确的是( )
| A. | 通入甲烷的电极为正极 | |
| B. | 电池工作一段时间后,溶液的碱性增强 | |
| C. | 负极的电极反应:CH4+l0OH--8e-=CO32-+7H2O | |
| D. | 通入甲烷的电极的电极反应:O2+2H2O+4e-=4OH- |
7.下列实验方案能达到目的是( )
| A. | 除去Fe粉中混有的I2:加热使I2升华 | |
| B. | 除去NaCl固体中混有的MgCl2:加入KOH溶液后过滤,滤液蒸发结晶 | |
| C. | 除去碳酸钠中混有的碳酸氢钠:加入过量的氢氧化钠溶液,蒸发结晶 | |
| D. | 除去氯气中含有的氯化氢气体:用饱和食盐水洗涤后干燥 |
8.下列叙述中,表明金属甲的活泼性比金属乙的活泼性强的是( )
| A. | 在氧化还原反应中,甲比乙失电子多 | |
| B. | 同价态的阳离子,甲比乙氧化性强 | |
| C. | 甲能与稀硫酸反应生成氢气而乙不能 | |
| D. | 甲的最高价氧化物的水化物的碱性弱 |
