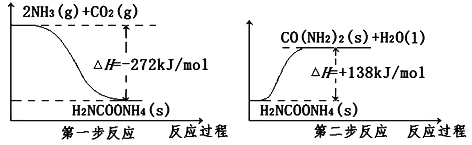
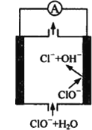
题目内容
【题目】在一定条件下,对于反应mA(g)+nB(g) ![]() cC(g)+dD(g),C物质的质量分数(C%)随温度升高或压强增大而减小。下列判断正确的是
cC(g)+dD(g),C物质的质量分数(C%)随温度升高或压强增大而减小。下列判断正确的是
A. 该反应为放热反应
B. (m+n) >(c+d)
C. 减小压强,平衡正向移动,平衡常数K值增大
D. 达到平衡后,增加A的物质的量,平衡正向移动,A的转化率增大
【答案】A
【解析】C物质的质量分数(C%)随温度升高而减小,说明升高温度平衡逆向移动,所以该反应为放热反应,故A正确;C物质的质量分数(C%)随压强增大而减小,说明增大压强平衡逆向移动,所以(m+n) <(c+d),故B错误;平衡常数只与温度有关,减小压强,平衡正向移动,平衡常数K值不变,故C错误;达到平衡后,增加A的物质的量,平衡正向移动,A的转化率减小,B的转化率增大,故D错误。

【题目】某化学小组同学用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件。
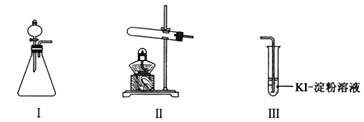
供选试剂:30% H2O2溶液、0.1mol/L H2SO4溶液、MnO2固体、KMnO4固体。
(1)小组同学设计甲、乙、丙三组实验,记录如下:
操作 | 现象 | |
甲 | 向I的锥形瓶中加入______,向I的______中加入30% H2O2溶液,连接I、Ⅲ,打开活塞 | I中产生无色气体并伴随大量白雾;Ⅲ中有气泡冒出,溶液迅速变蓝 |
乙 | 向Ⅱ中加入KMnO4固体,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液不变蓝 |
丙 | 向Ⅱ中加入KMnO4固体,Ⅲ中加入适量0.1mol/L H2SO4溶液,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液变蓝 |
(2)丙实验中O2与KI溶液反应的离子方程式是__________________________。
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是___________。为进一步探究该条件对反应速率的影响,可采取的实验措施是________________________。
(4)由甲、乙、丙三实验推测,甲实验可能是I中的白雾使溶液变蓝。学生将I中产生的气体直接通入下列________溶液(填序号),证明了白雾中含有H2O2。
A.酸性KMnO4 B.FeCl2 C.氢硫酸 D.品红
(5)资料显示:KI溶液在空气中久置过程中会被缓慢氧化:4KI +O2 +2H2O=2I2 + 4KOH。该小组同学取20 mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应(写离子方程式)_____________________造成的,请设计实验证明他们的猜想是否正确。_________________________________________。