题目内容
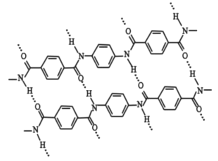
【题目】如图为某“导电分子线”的结构,下列对该有机分子的说法,正确的是( )
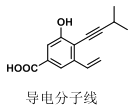
A.最多有 7 个原子共线
B.最多有 13 个碳原子共面
C.可发生加成、酯化、消去反应
D.不考虑立体异构,该分子中共有 7 种化学环境不同的氢
【答案】B
【解析】
A.从图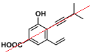 中可以看出,共线的碳原子位于红线上,最多有 6 个,A不正确;
中可以看出,共线的碳原子位于红线上,最多有 6 个,A不正确;
B.从图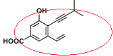 中可以看出,本环中所有碳原子、乙烯基双键碳原子(=CH2中碳原子)、2个-CH3中只能有1个碳原子与其它基团中碳原子可能共面,所以共面的碳原子最多有 13 个,B正确;
中可以看出,本环中所有碳原子、乙烯基双键碳原子(=CH2中碳原子)、2个-CH3中只能有1个碳原子与其它基团中碳原子可能共面,所以共面的碳原子最多有 13 个,B正确;
C.该有机物中含有碳碳三键,可发生加成反应,含有羧基,可发生酯化反应,但不能发生消去反应,C不正确;
D.该有机物分子中,只有2个-CH3上的氢原子化学环境相同,不考虑立体异构,该分子中共有 8 种化学环境不同的氢,D不正确;
故选B。

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向盛有某盐溶液的试管中滴入氢氧化钠溶液后,加热,试管口处湿润的红色石蕊试纸变蓝 | 该盐中含 |
B | 向溴水中通入某无色气体,溴水褪色 | 该气体可能是CH2=CH2 |
C | 一定量的铜与硝酸充分反应后,有铜剩余,再加入少量稀硫酸,铜继续溶解,并有气泡放出 | Cu与稀硫酸发生了反应 |
D | 向淀粉溶液中加少量稀硫酸,加热4~5min。冷却后向其中加入新制Cu(OH)2悬浊液,加热至沸腾,无砖红色沉淀 | 淀粉没有发生水解 |
A.AB.BC.CD.D