题目内容
【题目】诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂。工高温业上冶炼钼的化学反应过程为①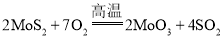 ;②
;②![]() ;③
;③![]() ;④
;④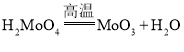 ;⑤用还原剂将
;⑤用还原剂将![]() 还原成金属钼。下列说法正确的是( )
还原成金属钼。下列说法正确的是( )
A.![]() 煅烧产生的尾气可直接排放
煅烧产生的尾气可直接排放
B.![]() 是金属氧化物,也是碱性氧化物
是金属氧化物,也是碱性氧化物
C.![]() 是一种强酸
是一种强酸
D.利用![]() 、
、![]() 和
和![]() 分别还原等量的
分别还原等量的![]() ,所消耗还原剂的物质的量之比为
,所消耗还原剂的物质的量之比为![]()
【答案】D
【解析】
A.生成物![]() 对环境污染严重,不可直接排放,A错误;
对环境污染严重,不可直接排放,A错误;
B.②中![]() 与碱反应生成盐
与碱反应生成盐![]() 和水,符合酸性氧化物的定义,故
和水,符合酸性氧化物的定义,故![]() 不属于碱性氧化物, B错误;
不属于碱性氧化物, B错误;
C.由反应③可知,![]() 是一种不溶性酸,故
是一种不溶性酸,故![]() 不可能是强酸, C错误;
不可能是强酸, C错误;
D.![]() 、
、![]() 和
和![]() 作还原剂时,失去的电子分别为2 mol、2 mol和3 mol,则还原等量的
作还原剂时,失去的电子分别为2 mol、2 mol和3 mol,则还原等量的![]() 时,转移电子数相同,此时消耗的
时,转移电子数相同,此时消耗的![]() ,D正确;
,D正确;
答案选D。

【题目】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:0.5 ℃,有毒)常温下是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成,并以液态储存。

(1)甲组的同学拟制备原料气NO和Cl2,均采用上图制备装置:
①写出NOCl的N元素化合价:_______
②为制备纯净干燥的气体,下表中缺少的药品是(填写在横线上):
实验项目 | 装置Ⅰ | 装置Ⅱ | |
制备的气体 | 烧瓶中 | 分液漏斗中 | |
a .制备纯净干燥的Cl2 | MnO2 | _______ | _______ |
b .制备纯净干燥的NO | Cu | _______ | _______ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
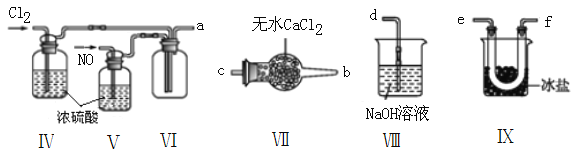
①装置连接顺序为a→____________________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是______________________________。
③装置Ⅵ在实验结束,拆解装置前,应作怎样的处理?_________________________。
④装置Ⅷ中吸收尾气时,NOCl发生的非氧化还原反应的化学方程式为___________________。
【题目】一定温度下,在1L恒容密闭容器中加入lmol的N2(g)和3molH2(g)发生反应:N2(g)+3H2(g) ![]() 2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法不正确的是( )
2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法不正确的是( )
时间(min) | 0 | t1 | t2 | t3 |
NH3物质的量(mol) | 0 | 0.2 | 0.3 | 0.3 |
A. 0t1min,v(NH3)=0.2/t1mol·L-1·min-1
B. t3时再加入1mol的N2(g)和3molH2(g),反应达新平衡时,c(N2)>0.85mol·L-1
C. N2(g)+3H2(g) ![]() 2NH3(g)的活化能小于2NH3(g)
2NH3(g)的活化能小于2NH3(g) ![]() N2(g)+3H2(g)的活化能
N2(g)+3H2(g)的活化能
D. 升高温度,可使正反应速率减小,逆反应速率增大,故平衡逆移