题目内容
(9分)
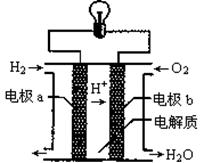
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为 、 。
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是 ,电解氯化钠溶液的总反应方程式为 ;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为
(法拉第常数F=9.65×l04C.mol-1,列式计算),最多能产生的氯气体积为 L(标准状况)。
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为 、 。
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是 ,电解氯化钠溶液的总反应方程式为 ;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上通过电解池的电量为
(法拉第常数F=9.65×l04C.mol-1,列式计算),最多能产生的氯气体积为 L(标准状况)。
:(1)O2+2H2O +4e—=4OH—,CH4+10OH--8e—=CO32-+ 7H2O;(2)H2;2NaCl+2H2O 2NaOH+ H2↑+ Cl2↑;(3)(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;4。
2NaOH+ H2↑+ Cl2↑;(3)(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;4。
 2NaOH+ H2↑+ Cl2↑;(3)(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;4。
2NaOH+ H2↑+ Cl2↑;(3)(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;4。:(1)燃料电池的总反应就是燃料燃烧的反应即:CH4+2O2+2OH- = CO32-+ 3H2O,故其正极反应式为:O2+ 2H2O +4e—= 4OH—,我们用总反应式减正极反应式可得负极反应式:CH4+10OH--8e—=CO32-+ 7H2O;(2分析图中三池可看出1、2两池是串联的燃料电池,通入甲烷的一极是负极,故此电解池中与其相连的b电极为阴极,生成的气体为氢气;电解的总反应式为:2NaCl+2H2O 2NaOH+ H2↑+ Cl2↑;(3)根据(1)中的负极反应式,可知通入1mol甲烷时失电子8mol,总电量为8×96500C,由于图中的两个电池是串联,故可知线路上转移的电子与一个燃料电池时相同,结合甲烷的量,其1L为1/22.4mol,可求电为:(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;电解时得到氢气为4L。
2NaOH+ H2↑+ Cl2↑;(3)根据(1)中的负极反应式,可知通入1mol甲烷时失电子8mol,总电量为8×96500C,由于图中的两个电池是串联,故可知线路上转移的电子与一个燃料电池时相同,结合甲烷的量,其1L为1/22.4mol,可求电为:(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;电解时得到氢气为4L。
【考点定位】此题以燃料电池的使用为载体,考查了原电池的电极反应式书写、电极的判断和电解知识。
 2NaOH+ H2↑+ Cl2↑;(3)根据(1)中的负极反应式,可知通入1mol甲烷时失电子8mol,总电量为8×96500C,由于图中的两个电池是串联,故可知线路上转移的电子与一个燃料电池时相同,结合甲烷的量,其1L为1/22.4mol,可求电为:(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;电解时得到氢气为4L。
2NaOH+ H2↑+ Cl2↑;(3)根据(1)中的负极反应式,可知通入1mol甲烷时失电子8mol,总电量为8×96500C,由于图中的两个电池是串联,故可知线路上转移的电子与一个燃料电池时相同,结合甲烷的量,其1L为1/22.4mol,可求电为:(1L/22.4L.mol-1)×8×9.65× 104C.mol-1 =3.45×104C;电解时得到氢气为4L。【考点定位】此题以燃料电池的使用为载体,考查了原电池的电极反应式书写、电极的判断和电解知识。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

 是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题: