题目内容
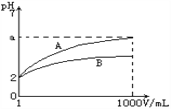
【题目】pH=2的A、B两种酸溶液各lmL,分别加水稀释到1000 mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是( )
A. A、B两种酸溶液物质的量浓度一定相等
B. 稀释后A酸溶液的酸性比B酸溶液强
C. a=5时,A是强酸,B是弱酸
D. 若A、B都是弱酸,则5≥a>2
【答案】C
【解析】A、等pH的酸加水稀释,酸性强的pH变化大。起始时pH相等,但两种酸的强弱未知,所以物质的量浓度不一定相等,A错误;B、稀释后A酸溶液pH大,c(H+)小,酸性弱,B错误;C、若a=5,稀释1000倍后,A酸溶液的pH=5,B酸溶液的pH小于5,则A是强酸、B是弱酸,C正确;D、若A、B均是弱酸,则2<a<5,D错误,答案选C。

练习册系列答案
相关题目