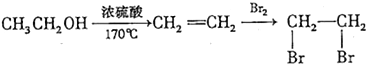题目内容
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
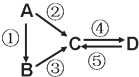
(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出②反应的离子方程式_________;④反应离子方程式__________。
(2)若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水高温下反应的化学方程式_______________________。④反应的离子方程式______________。D中加入氢氧化钠的现象__________。
(3)若A是太阳能电池用的光伏材料,B常用用于制作高档光学器材,C、D为钠盐,C的水溶液俗称泡花碱,D的溶液显碱性。④反应也是通入一种引起温室效应的主要气体。写出③反应的化学方程式________________________。⑤反应用到B,反应条件为高温,则⑤的化学方程式为____________________。
【答案】2Al+2OH-+2H2O=2AlO2-+3H2↑AlO2-+CO2(过量)+2H2O=Al(OH)3↓+HCO3-3Fe+4H2O(g)![]() Fe3O4+4H2Fe+2Fe3+=3Fe2+生成的白色沉淀迅速变成灰绿色,最后变成红褐色SiO2+2NaOH=Na2SiO3+H2OSiO2+Na2CO3
Fe3O4+4H2Fe+2Fe3+=3Fe2+生成的白色沉淀迅速变成灰绿色,最后变成红褐色SiO2+2NaOH=Na2SiO3+H2OSiO2+Na2CO3![]() Na2SiO3+CO2↑
Na2SiO3+CO2↑
【解析】
(1)若D物质具有两性,推断D为Al(OH)3,④反应是通入过量的一种引起温室效应的主要气体,气体是二氧化碳,说明C为偏铝酸钠,②③反应均要用强碱溶液,判断A为Al,B为铝盐,则②反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,④反应离子方程式为AlO2-+CO2(过量)+2H2O=Al(OH)3↓+HCO3-;
(2)若A是应用最广泛的金属,A为Fe,铁与水高温下反应的化学方程式为3Fe+4H2O(g)![]() Fe3O4+4H2;④反应用到A,②⑤反应均用到同一种黄绿色气体单质,推断为Cl2,则C为FeCl3,D为FeCl2,因此④反应的离子方程式为Fe+2Fe3+=3Fe2+;氯化亚铁中加入氢氧化钠的现象为生成的白色沉淀迅速变成灰绿色,最后变成红褐色;
Fe3O4+4H2;④反应用到A,②⑤反应均用到同一种黄绿色气体单质,推断为Cl2,则C为FeCl3,D为FeCl2,因此④反应的离子方程式为Fe+2Fe3+=3Fe2+;氯化亚铁中加入氢氧化钠的现象为生成的白色沉淀迅速变成灰绿色,最后变成红褐色;
(3)若A是太阳能电池用的光伏材料,判断A为Si。B常用用于制作高档光学器材,B是二氧化硅。C、D为钠盐,C的水溶液俗称泡花碱,C是硅酸钠,D的溶液显碱性,④反应也是通入一种引起温室效应的主要气体,即二氧化碳,所以D是碳酸钠。根据以上分析可知③反应的化学方程式为SiO2+2NaOH=Na2SiO3+H2O。⑤反应用到B,反应条件为高温,则⑤的化学方程式为SiO2+Na2CO3![]() Na2SiO3+CO2↑。
Na2SiO3+CO2↑。

【题目】向2 L密闭容器中加入一定量的固体A和气体B,发生反应A(s)+2B(g) ![]() D(g)+E(g)ΔH=Q kJ·mol-1。在T1 ℃时,反应进行到不同时间测得各物质的物质的量如表:
D(g)+E(g)ΔH=Q kJ·mol-1。在T1 ℃时,反应进行到不同时间测得各物质的物质的量如表:
时间(min) 物质的量(mol) | 0 | 10 | 20 | 30 | 40 | 50 |
B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
(1)T ℃时,该反应的平衡常数K=____________________________。
(2)30 min后,只改变某一条件,反应重新达到平衡,据表中数据判断改变的条件可能是_____(填编号)。
a.通入一定量的B b.加入一定量的固体A c.适当缩小容器的体积
d.升高反应体系温度 e.同时加入0.2 mol B、0.1 mol D、0.1 mol E
(3)对于该反应,用各物质表示的反应速率与时间的关系示意曲线为下图中的____________(填序号)。
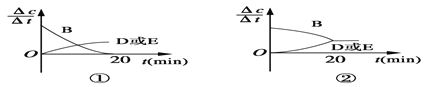
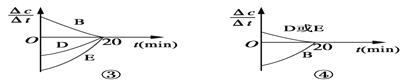
(4)容器的体积和温度T1 ℃不变,向该容器中加入1.60 mol B、0.20 mol D、0.20 mol E和n mol A,达到平衡后,与表格中20分钟时各物质的浓度完全相同,投入固体A的物质的量n的取值范围是______。
(5)若该密闭容器绝热,实验测得B的转化率随温度变化的示意图如图所示。由图可知,Q________0(填“大于”或“小于”),c点v正________v逆(填“大于”、“小于”或“等于”)。

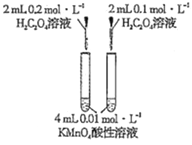
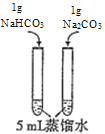
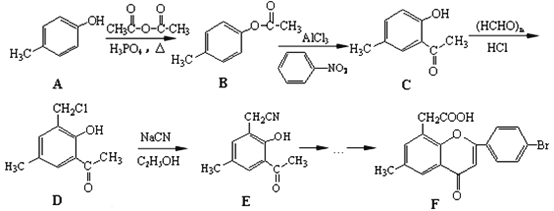
【题目】下列实验方案中不能达到相应实验目的的是
选项 | A | B | C | D |
方案 |
|
|
|
|
目的 | 探究浓度对化学反应速率的影响 | 探究催化剂对H2O2分解速率的影响 | 室温下比较NaHCO3和Na2CO3的溶解度 | 探究温度对化学平衡的影响 |
A. A B. B C. C D. D