题目内容
【题目】为了证明一氧化碳具有还原性,有人设计了下列实验:
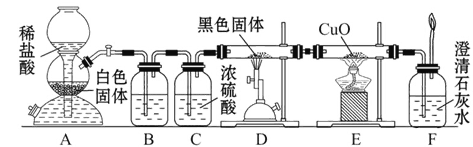
(1)装置A中生成的主要产物是___________________________________________。
(2)装置D中发生反应的化学方程式是___________________________________。
(3)必须用装置C吸收除去气体中水蒸气的理由是_________________________。
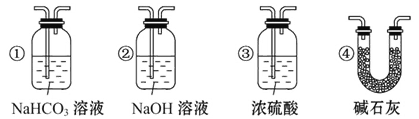
(4)若根据F中石灰水变浑浊的现象也能确定CO具有还原性,应在上图中装置______与______之间连接下列装置中的______(填序号)。
【答案】CO2 CO 2 +C![]() 2CO 水蒸气进入D中在高温下能跟碳反应产生H 2 ,H 2 也能使CuO还原,不能证明CO具有还原性 D E ④
2CO 水蒸气进入D中在高温下能跟碳反应产生H 2 ,H 2 也能使CuO还原,不能证明CO具有还原性 D E ④
【解析】
利用一氧化碳还原氧化铜证明一氧化碳具有还原性。一氧化碳可以由二氧化碳和碳反应制得,所以需要首先制取二氧化碳。用稀盐酸和大理石制取二氧化碳,通过饱和碳酸氢钠溶液除去二氧化碳里的氯化氢,再通过浓硫酸除去水蒸气,通入装有碳的硬质玻璃管,得到的一氧化碳还原氧化铜,生成的二氧化碳能使石灰水变浑浊,多余的一氧化碳可以点燃除去。
根据上述
(1)装置A中生成的主要产物是CO2。
(2)装置D中发生反应的化学方程式是CO 2 +C![]() 2CO。
2CO。
(3)水蒸气进入D中在高温下能跟碳反应产生H 2 ,H 2 也能使CuO还原,不能证明CO具有还原性,所以必须用装置C吸收除去气体中水蒸气。
(4)二氧化碳通过碳,不能全部和碳反应,剩余的二氧化碳进入F中,也能使石灰水变浑浊。若要证明CO的还原性,就必须除去剩余的CO2,所以应在上图中装置D与E之间连接一个可以除去二氧化碳同时又不能带入水蒸气的装置,故选④。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目