题目内容
【题目】向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)![]() SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是( )
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。由图可得出的正确结论是( )
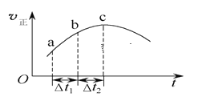
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.反应物的总能量高于生成物的总能量
D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段
【答案】CD
【解析】
由题意可知一个反应前后体积不变的可逆反应,由于容器恒容,因此压强不影响反应速率,所以在本题中只考虑温度和浓度的影响。结合图象可知反应速率先增大再减小,因为只要开始反应,反应物浓度就要降低,正反应速率应该降低,但此时正反应速率却是升高的,这说明此时温度的影响是主要的,由于容器是绝热的,因此该反应是放热反应,从而导致容器内温度升高反应速率加快,而在c点之后,正反应速率降低,而温度是升高的,说明浓度是主要因素。
A、化学平衡状态的标志是各物质的浓度不再改变,其实质是正反应速率等于逆反应速率,c点对应的正反应速率显然还在改变,故一定未达平衡,故A错误;
B、a到b时正反应速率增加,反应物浓度随时间不断减小,a点反应物的大于b点,故B错误;
C、从a到c正反应速率增大,c点之后正反应速率减小,说明反应刚开始时温度升高对正反应速率的影响大于浓度减小对正反应速率的影响,说明该反应为放热反应,即反应物的总能量高于生成物的总能量,故C正确;
D、随着反应的进行,正反应速率越快,消耗的二氧化硫就越多。a~b段平均速率小于b~c段的平均速率,则b~c段SO2的转化率较大,故D正确;
故选:CD。

练习册系列答案
相关题目