题目内容
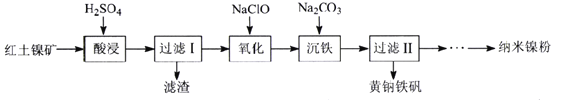
【题目】钒钢具有高强度、弹性优良、抗磨损、抗冲击等性能,可用于汽车和飞机制造。一种从石煤(含SiO2、V2O3、V2O5和少量Fe2O3)中提取V2O5的流程如下图所示:
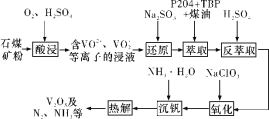
已知:
VO2+ | VO2+ | Fe2+ | Fe3+ | |
P2O4+TBP+煤油中的溶解度 | 很大 | 较小 | 0 | 很大 |
请回答下列问题:
(1)“酸浸”时,为提高浸出速率,除适当增加硫酸浓度、减小石煤矿粉粒径外,还可采取的措施有__________(任写一条);生成VO2+反应的离子方程式为_______。
(2)从整个流程来看,“还原”的目的为_______。
(3)实验室模拟“萃取”时,需用到的玻璃仪器有____________。
(4)“氧化”时发生反应的离子方程式为__________。
(5)上述流程中可以循环利用的物质有_________。
(6)全钒液流储能电池的工作原理为VO2++V3++H2O![]() VO2++V2++2H+。
VO2++V2++2H+。
①充电时,阳极的电极反应式为______;
②两极区被质子交换膜隔开,放电时,若外电路转移2mole-,则正极区溶液中n(H+)________(填“增加”或“减少”)________mol。
【答案】适当升高反应温度、适当增大O2通入量、搅拌(其他合理答案均可,任写一条) 2V2O3+8H++O2=4VO2++4H2O 将VO2+还原为VO2+、Fe3+还原为Fe2+,利于后续萃取分离 分液漏斗、烧杯 6VO2++ClO3-+3H2O=6VO2++Cl-+6H+ P2O4+TBP+煤油、NH3(或NH3·H2O) VO2+-e-+H2O=VO2++2H+ 减少 2
【解析】
石煤(含SiO2、V2O3、V2O5和少量Fe2O3)与硫酸和氧气反应生成的主要是含有VO2+、VO2+、Fe3+,经过亚硫酸钠还原,变为VO2+、Fe2+,经过P2O4+TBP+煤油的萃取出VO2+,再用硫酸反萃取出VO2+,经过NaClO3的氧化,再加氨水沉钒,再热解得到V2O5。
⑴由流程图可知,“酸浸”时需加入O2和H2SO4,为加快反应速率,除了适当增加硫酸浓度、减小石煤矿粉粒径外,还可采取适当升高反应温度、适当增大O2通入量、搅拌等措施;生成VO2+反应的离子方程式为2V2O3+8H++O2 = 4VO2++4H2O;故答案为:适当升高反应温度、适当增大O2通入量、搅拌(其他合理答案均可,任写一条);2V2O3+8H++O2=4VO2++4H2O。
⑵分析反应流程及表格数据可知,VO2+与Fe3+在P2O4+TBP+煤油中的溶解度很大,而VO2+与Fe2+在萃取剂中的溶解度较小,要除去含铁杂质,可将VO2+还原为VO2+、Fe3+还原为Fe2+,利于后续萃取分离;故答案为:将VO2+还原为VO2+、Fe3+还原为Fe2+,利于后续萃取分离。
⑶在“萃取”操作中,需用到的玻璃仪器有分液漏斗、烧杯;故答案为:分液漏斗、烧杯。
⑷“氧化”过程为加入NaClO3将VO2+氧化为VO2+,发生反应的离子方程式为6VO2++ClO3-+3H2O = 6 VO2++Cl-+6H+;故答案为:6VO2++ClO3-+3H2O = 6 VO2++Cl-+6H+。
⑸由流程图可知,该流程进行了“萃取”与“反萃取”,故萃取剂P2O4+TBP+煤油可循环使用,另外“热解”产生的NH3可配制成NH3·H2O溶液,用于“沉钒”操作;故答案为:P2O4+TBP+煤油、NH3(或NH3·H2O)。
⑹①充电时阳极发生氧化反应,其电极反应式应为VO2+-e-+H2O = VO2++2H+。②放电时正极反应式为VO2++e-+2H+= VO2++H2O,负极反应式为V2+-e-=V3+,故当外电路转移2mole-时,正极反应消耗4molH+,负极区有2molH+通过质子交换膜移向正极区,故正极区溶液中n(H+)将减少2mol;故答案为:VO2+-e-+H2O=VO2++2H+;减少;2。

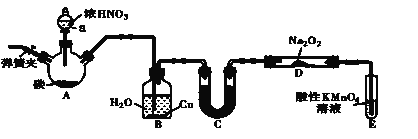
【题目】![]() 是一种常见的化学试剂,是制备其他含锰化合物的重要原料。某课外化学兴趣小组利用软锰矿
是一种常见的化学试剂,是制备其他含锰化合物的重要原料。某课外化学兴趣小组利用软锰矿![]() 主要成分为
主要成分为![]() ,含少量
,含少量![]() 、
、![]() 和
和![]() 制备
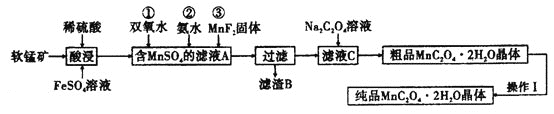
制备![]() ,设计流程如图:
,设计流程如图:![]() 注:试剂①②③按编号顺序加入
注:试剂①②③按编号顺序加入![]()
已知:常温时部分难溶化合物的![]() 近似值
近似值![]() 如表:
如表:
物质 |
|
|
|
|
|
|
|
|
|
|
|
(1)该小组同学在酸浸之前,先将软锰矿粉碎,其目的是________。
(2)“酸浸”过程中![]() 发生反应的离子方程式为________。
发生反应的离子方程式为________。
(3)加入![]() 固体的作用是________,甲同学提出将上述流程中的氨水换成氢氧化钠溶液,乙同学觉得不妥,乙同学的理由是________。
固体的作用是________,甲同学提出将上述流程中的氨水换成氢氧化钠溶液,乙同学觉得不妥,乙同学的理由是________。
(4)丙同学认为向滤液C中滴加![]() 溶液的过程中可能会生成
溶液的过程中可能会生成![]() 沉淀,并提出可能的原因为
沉淀,并提出可能的原因为![]() ,常温时,该反应的平衡常数
,常温时,该反应的平衡常数![]() ________
________![]() 填数值
填数值![]() 。
。![]() 已知
已知![]() ,
,![]() 。
。
(5)操作Ⅰ的名称为________。
(6)如图是小组同学将![]() 晶体放在坩埚里加热分解时,固体失重质量分数随温度
晶体放在坩埚里加热分解时,固体失重质量分数随温度![]() 变化的曲线
变化的曲线![]() 已知草酸锰不稳定,但其中锰元素的化合价在
已知草酸锰不稳定,但其中锰元素的化合价在![]() 以下不变
以下不变![]() 。
。
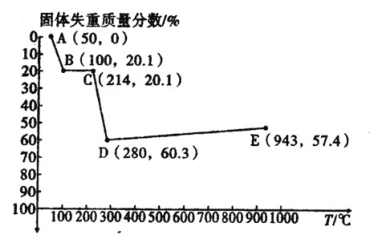
试根据各点的坐标![]() 近似值
近似值![]() 回答下列问题:
回答下列问题:
①![]() 的化学方程式为________。
的化学方程式为________。
②从D点到E点过程中固体失重的质量分数下降的原因是________。
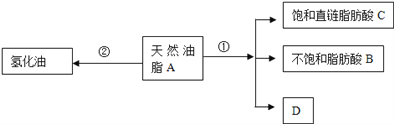
【题目】海洋动物海鞘中含有种类丰富、结构新颖的次生代谢产物,是海洋抗肿瘤活性物质的重要来源之一。一种从海鞘中提取具有抗肿瘤活性的天然产物的流程如下:
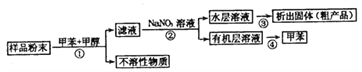
下列关于该流程中各步骤的说法中,错误的是( )
选项 | 步骤 | 采用装置 | 主要仪器 |
A | ① | 过滤装置 | 漏斗 |
B | ② | 分液装置 | 分液漏斗 |
C | ③ | 蒸发装置 | 坩埚 |
D | ④ | 蒸馏装置 | 蒸馏烧瓶 |
A. A B. B C. C D. D