��Ŀ����
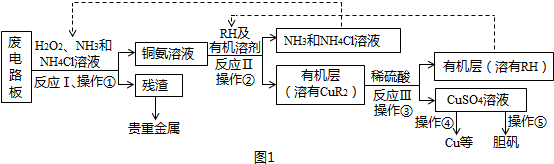
2��������F��һ�־��в�����ζ�ĸ��������ϳ�·�����£�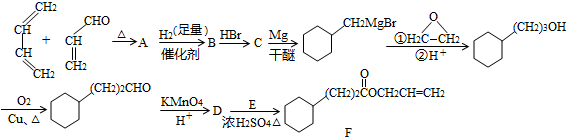
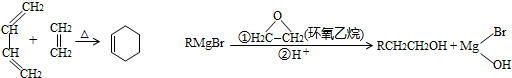
��֪
��1��A�Ľṹ��ʽΪ
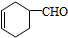 ��A�����������ŵ�������ȩ����̼̼˫����
��A�����������ŵ�������ȩ����̼̼˫������2����A����B�ķ�Ӧ�����Ǽӳɷ�Ӧ��E��ijͬ���칹��ֻ��һ����ͬ��ѧ�������⣬��ͬ���칹��Ľṹ��ʽΪ
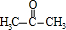 ��
�� ��3��д��D��E��Ӧ����F�Ļ�ѧ����ʽ
 ��
����4����������Ϣ����������ͻ�������Ϊԭ���Ʊ�1-��������ƺϳ�·�ߣ������Լ���ѡ����
�ϳ�·������ͼʾ����
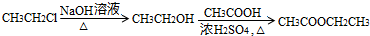
���� ������Ŀ������Ϣ����֪1��3-����ϩ���ϩȩ�����ӳɷ�Ӧ��Ӧ����AΪ ��A�����������������ӳɷ�Ӧ����BΪ
��A�����������������ӳɷ�Ӧ����BΪ ��B��HBr�����·���ȡ����Ӧ����CΪ
��B��HBr�����·���ȡ����Ӧ����CΪ ��C��Mg�ڸ��ѵ������µõ�
��C��Mg�ڸ��ѵ������µõ� ��
�� ������Ϣ�з�Ӧ�õ�
������Ϣ�з�Ӧ�õ�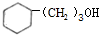 ���ٷ�����������Ӧ����
���ٷ�����������Ӧ����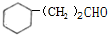 ��
��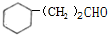 �����Ը��������Һ��Һ��������DΪ
�����Ը��������Һ��Һ��������DΪ ���Ա�D��F�Ľṹ��֪��D��CH2=CHCH2OH��Ӧ������Ӧ�õ�F����EΪCH2=CHCH2OH��
���Ա�D��F�Ľṹ��֪��D��CH2=CHCH2OH��Ӧ������Ӧ�õ�F����EΪCH2=CHCH2OH��
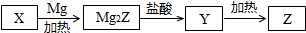
��4����ת����ϵ�з�Ӧ��֪����������Mg�ڸ��ѵ������µõ�CH3CH2MgBr�����뻷�����������������µõ�1-������
��� �⣺������Ŀ������Ϣ����֪1��3-����ϩ���ϩȩ�����ӳɷ�Ӧ��Ӧ����AΪ ��A�����������������ӳɷ�Ӧ����BΪ
��A�����������������ӳɷ�Ӧ����BΪ ��B��HBr�����·���ȡ����Ӧ����CΪ
��B��HBr�����·���ȡ����Ӧ����CΪ ��C��Mg�ڸ��ѵ������µõ�
��C��Mg�ڸ��ѵ������µõ� ��
�� ������Ϣ�з�Ӧ�õ�
������Ϣ�з�Ӧ�õ�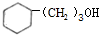 ���ٷ�����������Ӧ����
���ٷ�����������Ӧ����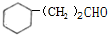 ��
��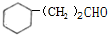 �����Ը��������Һ��Һ��������DΪ
�����Ը��������Һ��Һ��������DΪ ���Ա�D��F�Ľṹ��֪��D��CH2=CHCH2OH��Ӧ������Ӧ�õ�F����EΪCH2=CHCH2OH��
���Ա�D��F�Ľṹ��֪��D��CH2=CHCH2OH��Ӧ������Ӧ�õ�F����EΪCH2=CHCH2OH��
��1��������������֪��A�Ľṹ��ʽΪ �������������У�ȩ����̼̼˫����
�������������У�ȩ����̼̼˫����
�ʴ�Ϊ�� ��ȩ����̼̼˫����
��ȩ����̼̼˫����
��2����A����B�ķ�Ӧ�������ڼӳɷ�Ӧ��EΪCH2=CHCH2OH��E��ijͬ���칹��ֻ��һ����ͬ��ѧ�������⣬��ͬ���칹��Ľṹ��ʽΪ��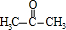 ��
��
�ʴ�Ϊ���ӳɷ�Ӧ��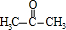 ��
��
��3��D��E��Ӧ����F�Ļ�ѧ����ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��4����ת����ϵ�з�Ӧ��֪����������Mg�ڸ��ѵ������µõ�CH3CH2MgBr�����뻷�����������������µõ�1-�������ϳ�·������ͼΪ��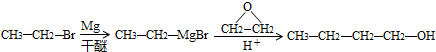 ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶ���ϳɣ��ɷ�����ת����ϵ���л���Ľ��н��з�����𣬽ϺõĿ���ѧ���ķ���������������ȡ��Ϣ������֪ʶǨ�������������Ѷ��еȣ�

| A�� | ҽԺ�������õ�����ˮ������Ҫ�ɷ���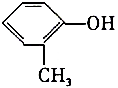 �������ڷ��� �������ڷ��� | |
| B�� | �����õĸ��ͣ�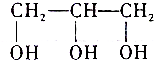 ��������Ԫ�� ��������Ԫ�� | |
| C�� | �����������õķ���Һ���Ҵ� | |
| D�� | ����-OH���ǻ��������ŵ��л��ﲻһ���Ǵ��� |
| A�� | ��ά�ء����ۡ�֬���������ʶ��Ǹ߷��ӻ����� | |
| B�� | ����ˮ������ղ��ﶼ�ܷ���������Ӧ | |
| C�� | ��ʳ�ؽ����ζ�������ж��ɷ��ô���������ţ�̽��н�� | |
| D�� | ֬���ܷ���������Ӧ�����ɸ��ͺ�֬������ |
��1���Ȼ�����ˮ���γɾ��о�ˮ���õ������������壬�䷴Ӧ�����ӷ���ʽΪAl3++3H2O?Al��OH��3+3H+��
��2����ҵ������������Ҫ�ɷ�ΪAl2O3������Fe2O3��SiO2�����ʣ���ȡ��ˮ�Ȼ�����һ�ֹ�������ʾ�����£�
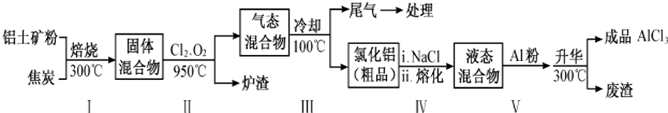
��֪��
| ���� | SiCl4 | AlCl3 | FeCl3 | FeCl2 |
| �е�/�� | 57.6 | 180�������� | 300�������� | 1023 |
�ڲ����������ͨ����������������Ӧ�������ԭ�������ȹ��ĵ�����Fe������
����֪��
Al2O3��s��+3C��s��=2Al��s��+3CO��g����H1=+1344.1kJ•mol-1
2AlCl3��g��=2Al��s��+3Cl2��g����H2=+1169.2kJ•mol-1
��Al2O3��C��Cl2��Ӧ����AlCl3���Ȼ�ѧ����ʽΪAl2O3��s��+3C��s��+3Cl2��g��=2AlCl3��g����+3CO��g����H=+174.9KJ/mol��
�ܲ����ľ���ȴ�����º�������������NaOH����Һ���գ����ɵ�����Ҫ��3�֣��仯ѧʽ�ֱ�ΪNaCl��NaClO��Na2CO3 ��
�ݽ�����̼�������ݷ�����������м������۵�Ŀ���dz�ȥFeCl3�����AlCl3���ȣ�
| A�� | +3 | B�� | +4 | C�� | +5 | D�� | +6 |
 ֱ�Ӽ״�ȼ�ϵ�����乩��������ʱ�䳤�����߷�չǰ�����乤��ԭ����ͼ��ʾ�����й�������˵����ȷ���ǣ�������
ֱ�Ӽ״�ȼ�ϵ�����乩��������ʱ�䳤�����߷�չǰ�����乤��ԭ����ͼ��ʾ�����й�������˵����ȷ���ǣ�������| A�� | ���Ӿ����·��b������a�� | |
| B�� | b���ĵ缫�뷴ӦΪO2+4e-+4H+=2H2O | |
| C�� | ���ӽ���Ĥ�е�H+����a�� | |
| D�� | �Դ˵�ع��磬���CuSO4��Һ��������ÿ����0.1molCu������Ҫ����1.12L |
 ��
��