题目内容
采用下列装置和操作,能达到实验目的的是

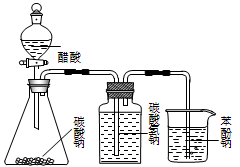
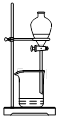

甲 乙 丙 丁




甲 乙 丙 丁
| A.甲装置:加热浓硫酸和乙醇(其体积为比3∶1)混合液,制取乙烯 |
| B.乙装置:比较醋酸、碳酸、苯酚三者的酸性强弱 |
| C.丙装置:向混有苯酚的苯中加入NaOH溶液,除去其中的苯酚 |
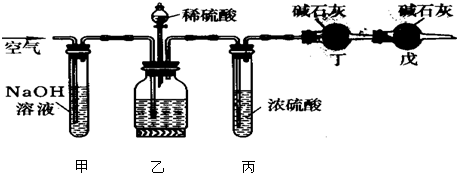
| D.丁装置:A中为乙醇、醋酸,B为饱和碳酸钠溶液,制取乙酸乙酯 |
BC
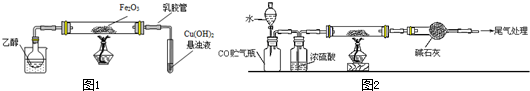
试题分析:A、实验室制取乙烯时需要控制溶液的温度为170℃,水银球应该放在溶液中,A不正确;B、醋酸与碳酸钙反应生成CO2,通入饱和的碳酸氢钠溶液中除去挥发出的乙酸,然后通入到苯酚钠溶液中生成苯酚,因此乙装置:比较醋酸、碳酸、苯酚三者的酸性强弱,B制取;C、苯酚能与氢氧化钠溶液反应,苯与氢氧化钠溶液反应,因此丙装置:向混有苯酚的苯中加入NaOH溶液,除去其中的苯酚,C制取;D、制取乙酸乙酯时需要浓硫酸作催化剂和吸水剂,D不正确,答案选BC。

练习册系列答案
 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
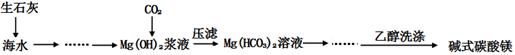
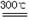 (x+y)MgO+xCO2↑+(y+z)H2O
(x+y)MgO+xCO2↑+(y+z)H2O =S↓ +SO2↑ +H2O
=S↓ +SO2↑ +H2O