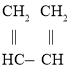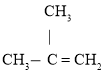题目内容
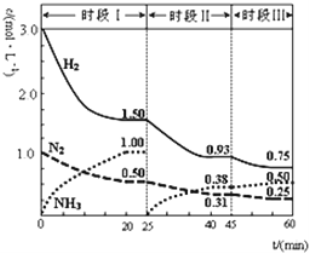
【题目】常温下,用0.100molL-1的NH4SCN溶液滴定25.00mL0.100molL-1AgNO3溶液,以NH4Fe(SO4)212H2O为指示剂,测得溶液中pSCN=lgc(SCN-)、pAg=lgc(Ag+)随加入NH4SCN溶液的体积变化如图所示。已知:Ag++SCN-AgSCN↓,Ksp(Ag2SO4)=1.4×10-5。下列说法错误的是( )

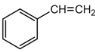
A.滴定至终点时溶液颜色变为红色,且振荡后不褪色
B.该温度下AgSCN的溶度积常数Ksp=1.0×10-12
C.为防止指示剂失效,溶液应维持酸性
D.当加入15.00mLNH4SCN溶液时,溶液中c(SO42-)=0.14molL-1
【答案】D
【解析】
A.达到终点后,![]() 与
与![]() 反应生成血红色物质,故滴定至终点时溶液颜色变为红色,且振荡后不褪色,故A正确;
反应生成血红色物质,故滴定至终点时溶液颜色变为红色,且振荡后不褪色,故A正确;
B.由图计算知该温度下AgSCN的溶度积常数![]() ,故B正确;
,故B正确;
C.由于碱性时,![]() 会沉淀,为防止指示剂失效,溶液应维持酸性,故C正确;
会沉淀,为防止指示剂失效,溶液应维持酸性,故C正确;
D.当加入![]() 溶液时,溶液中
溶液时,溶液中![]() ,此时
,此时![]() ,故D错误;
,故D错误;

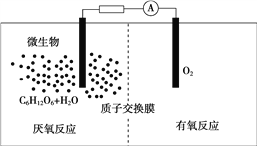
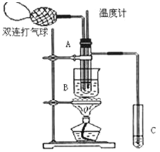
【题目】乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下表
物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
请回答下列问题:
(1)试管A内在60~80℃时发生的主要反应的化学方程式为(注明反应条件)________________________;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在________________________________,目的是________________________;当试管A内的主要反应完成后温度计水银球的位置应在________________,目的是________。
(3)烧杯B的作用是________;烧杯B内盛装的液体可以是________(写出一种即可,在题给物质中找)
(4)写出乙酸和碳酸氢钠反应的离子方程式________________________。