题目内容
关于反应2Fe3++Cu═2Fe2++Cu2+说法不正确的是( )
| A、该反应中Fe3+是氧化剂 |
| B、该反应中Cu被氧化了 |
| C、2mol Fe3+反应后共得到4NA个电子 |
| D、氧化产物与还原产物的物质的量之比为1:2 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:2Fe3++Cu═2Fe2++Cu2+中,Fe元素的化合价降低,Cu元素的化合价升高,以此来解答.
解答:
解:A.Fe元素的化合价降低,则该反应中Fe3+是氧化剂,故A正确;
B.Cu元素的化合价升高,失去电子被氧化,故B正确;
C.2mol Fe3+反应后得到电子为2mol,即共得到2NA个电子,故C错误;
D.Cu2+为氧化产物,Fe2+为还原产物,由反应可知,氧化产物与还原产物的物质的量之比为1:2,故D正确;
故选C.
B.Cu元素的化合价升高,失去电子被氧化,故B正确;
C.2mol Fe3+反应后得到电子为2mol,即共得到2NA个电子,故C错误;
D.Cu2+为氧化产物,Fe2+为还原产物,由反应可知,氧化产物与还原产物的物质的量之比为1:2,故D正确;
故选C.
点评:本题考查氧化还原反应,为高考常见题型,注意把握元素的化合价及反应中的变化为解答的关键,侧重基本概念和转移电子数的考查,题目难度不大.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
分子式为C4H7O2Br的有机物能与碳酸氢钠溶液反应产生气体,该有机物的结构可能有( )
| A、3种 | B、4种 | C、5种 | D、6种 |
为除去括号内的杂质,所选用的试剂或方法不正确的是( )
| A、NaHCO3溶液(Na2CO3溶液)通入过量的CO2 |
| B、铁粉(铝粉)加入适量的NaOH溶液过滤 |
| C、Na2CO3溶液(Na2SO4溶液)加入适量的Ba(OH)2溶液过滤 |
| D、CO2(CO)将混合气体通过足量灼热的CuO |
已知W、X、Y、Z为短周期元素,它们的原子半径依次增大,W与Z、X和Y分别同主族,Y、Z同周期.Z能与X形成两种常见的离子化合物,离子个数比均为2:1.下列说法错误的是( )
| A、Y、Z、X、W的原子序数依次减小 |
| B、W与X可形成既含极性共价键又含非极性共价键的化合物 |
| C、由W、X、Y、Z四种元素组成的常见化合物一定显酸性 |
| D、X的简单氢化物的沸点低于Y的简单氢化物的沸点 |
下列叙述正确的是( )
| A、在氧化还原反应中,金属单质一般只作还原剂 |
| B、氧化还原反应中非金属单质一定是氧化剂 |
| C、金属元素被还原时所得产物一定是金属单质 |
| D、某元素从化合态变为游离态,该元素一定被还原 |
把镁带投入盛有盐酸的敞口容器里,下列因素对反应速率有影响的是( )
①盐酸的浓度 ②镁带的表面积 ③溶液的温度 ④氯离子的浓度.
①盐酸的浓度 ②镁带的表面积 ③溶液的温度 ④氯离子的浓度.
| A、①② | B、③④ |
| C、①②③④ | D、①②③ |
NA代表阿伏加德罗常数,下列说法正确的是( )
| A、9g D2O中含有的电子数为5NA |
| B、92g NO2和N2O4混合气体中含有原子数为6NA |
| C、1mol C3H8分子中共价键总数为8NA |
| D、65g Zn全部溶解在一定浓度的硝酸溶液中,有NO生成,则转移的电子数为NA |
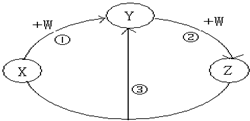 X、Y、Z、W都是中学化学常见的物质,其中X、Y、Z均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请按要求回答下列问题:
X、Y、Z、W都是中学化学常见的物质,其中X、Y、Z均含有同一种元素.在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去).请按要求回答下列问题: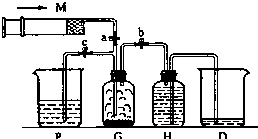 某课外活动小组利用下列装置迅速制备少量氯气.提供的试剂有:浓盐酸、饱和食盐水、氢氧化钠溶液、高锰酸钾固体.(2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O)试回答:
某课外活动小组利用下列装置迅速制备少量氯气.提供的试剂有:浓盐酸、饱和食盐水、氢氧化钠溶液、高锰酸钾固体.(2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O)试回答: