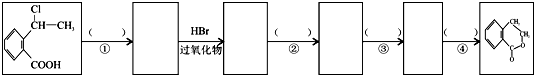
题目内容
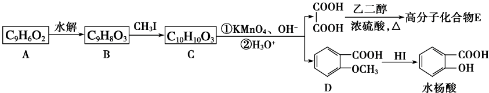
2.己烯雌酚是非甾体雄激素物质,可通过以下方法合成: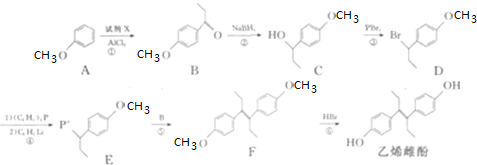
(1)化合物B中的含氧官能团为羰基、醚键(填名称);
(2)反应①中加入的试剂X的分子式为C3H5ClO,X的结构简式为
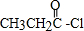 ;
;(3)上述反应①、②、③、⑥中,属于取代反应的是①③⑥(填序号);
(4)B的一种同分异构体满足下列条件:
①能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应;
②核磁共振氢谱有4个峰.该同分异构体的结构简式为
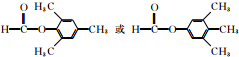 (任写一种).
(任写一种).(5)化合物
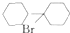 可由
可由 经五步反应合成:
经五步反应合成: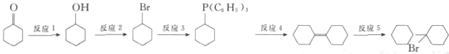
反应3的试剂为
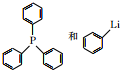 (写结构简式);
(写结构简式);反应2的化学方程为
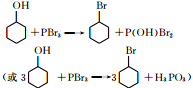 ;
;反应5的化学方程式为:
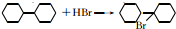 .
.
分析 反应①中加入的试剂X的分子式为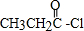 ,A发生取代反应生成B,根据A、B结构简式知,X结构简式为CH3CH2COCl,B和氢气发生加成反应生成C,C发生取代反应生成D,D发生取代反应生成E,E发生消去反应生成F,F发生取代反应生成乙烯雌酚,
,A发生取代反应生成B,根据A、B结构简式知,X结构简式为CH3CH2COCl,B和氢气发生加成反应生成C,C发生取代反应生成D,D发生取代反应生成E,E发生消去反应生成F,F发生取代反应生成乙烯雌酚,
(5)反应1为加成反应、反应2取代反应、反应3试剂为 、反应5为加成反应,据此分析解答.
、反应5为加成反应,据此分析解答.
解答 解:反应①中加入的试剂X的分子式为C3H5ClO,A发生取代反应生成B,根据A、B结构简式知,X结构简式为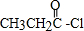 ,B和氢气发生加成反应生成C,C发生取代反应生成D,D发生取代反应生成E,E发生消去反应生成F,F发生取代反应生成乙烯雌酚.
,B和氢气发生加成反应生成C,C发生取代反应生成D,D发生取代反应生成E,E发生消去反应生成F,F发生取代反应生成乙烯雌酚.
(1)根据B结构简式知,化合物B中的含氧官能团为羰基、醚键,故答案为:羰基、醚键;
(2)反应①中加入的试剂X的分子式为C3H5ClO,X的结构简式为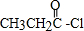 ,故答案为:
,故答案为: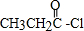 ,
,
(3)通过以上分析知,上述反应①、②、③、⑥中,属于取代反应的是①③⑥,故答案为:①③⑥;
(4)B的一种同分异构体满足下列条件:
①能发生银镜反应说明含有醛基,其水解产物之一能与FeCl3溶液发生显色反应说明水解产物之一含有酚羟基;
②核磁共振氢谱有4个峰说明该分子中氢原子种类有4种,
符合条件的该同分异构体的结构简式为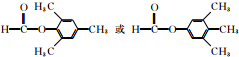 ,
,
故答案为: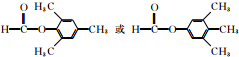 ;
;
(5)反应1为加成反应、反应2取代反应、反应3试剂为 、反应5为加成反应,
、反应5为加成反应,
反应3的试剂为 ,
,
反应2的化学方程为为 ;
;
反应5的化学方程式为: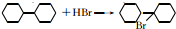 ;
;
故答案为: ;
; ;
;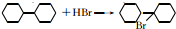 .
.
点评 本题考查有机合成,侧重考查学生分析判断能力,根据反应前后结构简式变化确定反应类型、断键和成键方式,知道常见有机物结构及其反应类型,题目难度不大.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
12.下列选项描述的过程能实现化学能转化成热能的是( )
| A. |  光合作用 | B. |  烧炭取暖 | C. |  风力发电 | D. |  电解冶炼 |
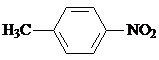
13.某碳、氢、氧有机物的蒸气密度是CO2的2倍(相同条件),它含有“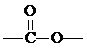 ”的同分异构体有( )
”的同分异构体有( )
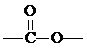 ”的同分异构体有( )
”的同分异构体有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 8种 |
17.25℃时,下列溶液的离子浓度关系式正确的是( )
| A. | pH=a的醋酸溶液稀释10倍后,其pH=b,则b=a+1 | |
| B. | 浓度相同的①NH4Cl;②CH3COONH4;③NH4HSO4三种溶液的c(NH4+):①>③>② | |
| C. | 浓度相同的氨水与盐酸等体积混合:c(NH4+)>c(Cl-)>c(H+)>c(OH-) | |
| D. | 将amol•L-1CH3COOH与bmol•L-1NaOH溶液等体积混合,测得溶液pH为7,则a>b |
7.下列说法正确的是( )
| A. | 某晶体固态不导电,水溶液能导电说明该晶体是离子晶体 | |
| B. | 原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力 | |
| C. | 分子组成相差一个或几个CH2原子团的有机物是同系物 | |
| D. | 在氢原子的基态电子的概率分布图中,小黑点的疏密程度表示电子在该区域空间出现概率的大小 |
14.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 为提高农作物的产量和质量,应大量使用化肥和农药 | |
| B. | 无论是风力发电还是火力发电,都是将化学能转化为电能 | |
| C. | PM2.5含有的铅、铬、钒、砷等对人体有害的金属元素 | |
| D. | 煤、石油、天然气是一级能源 |
11.下列是部分短周期中第二、第三周期元素的原子半径及主要化合价.
回答下列问题:
(1)⑧在元素周期表中的位置是(周期、族)第二周期第ⅥA族.
(2)8种元素的最高价氧化物的水化物中,酸性最强的是HClO4(填化学式).
(3)①元素和⑥元素形成化合物的电子式是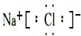 .
.
(4)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式:Al(OH)3+3H+═Al3++3H2O.
(5)下列叙述正确的是ABD(填字母).
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性.
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
(1)⑧在元素周期表中的位置是(周期、族)第二周期第ⅥA族.
(2)8种元素的最高价氧化物的水化物中,酸性最强的是HClO4(填化学式).
(3)①元素和⑥元素形成化合物的电子式是
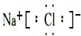 .
.(4)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式:Al(OH)3+3H+═Al3++3H2O.
(5)下列叙述正确的是ABD(填字母).
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性.
 .
.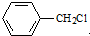 水解产物的同分异构体,且遇氯化铁溶液发生显色反应,写出X所有的可能结构简式:
水解产物的同分异构体,且遇氯化铁溶液发生显色反应,写出X所有的可能结构简式: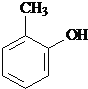 、
、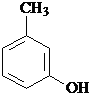 、
、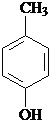 .
.
 .
.
 .
. .
.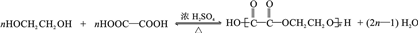 .
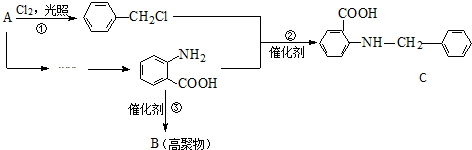
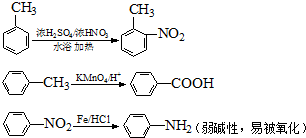
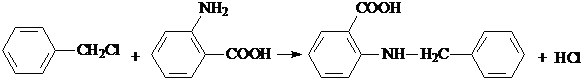
.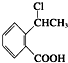 为原料制
为原料制 的合成路线流程图(无机试剂任用),在方框中填出相应的物质,并在括号注明反应条件.合成路线流程图示例如下:
的合成路线流程图(无机试剂任用),在方框中填出相应的物质,并在括号注明反应条件.合成路线流程图示例如下: