题目内容
6.水的电离过程为H2O?H++OH-,在不同温度下其离子积为Kw(25℃)=1.0×10-14,Kw(35℃)=2.1×10-14,则下列叙述中正确的是( )| A. | c(H+)随温度的升高而降低 | |
| B. | 35℃时,c(H+)>c(OH-) | |
| C. | 溶液pH:pH(35℃)>pH(25℃) | |
| D. | 35℃时已电离的水的浓度约为1.45×10-7 mol/L |
分析 水的电离过程为H2O?H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,KW(35℃)=2.1×10-14,说明升高温度促进水电离,升高温度后水中c(H+)增大,其pH减小,但仍然存在c(H+)=c(OH-),据此分析解答.
解答 解:水的电离过程为H2O?H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,KW(35℃)=2.1×10-14,说明升高温度促进水电离,升高温度后水中c(H+)增大,其pH减小,但仍然存在c(H+)=c(OH-),
A.升高温度促进水电离,则c(H+)随温度的升高而增大,故A错误;
B.升高温度促进水电离,但水中仍然存在c(H+)=c(OH-),呈中性,故B错误;
C.升高温度促进水电离,则c(H+)随温度的升高而增大,所以温度越高,水的pH越小,故C错误;
D.Kw(35℃)=2.1×10-14,35℃时已电离的水的浓度=$\sqrt{2.1×1{0}^{-14}}$=1.45×10-7 mol/L,故D正确;
故选D.
点评 本题考查水的电离,侧重考查学生获取信息、分析学习能力,知道离子积常数与温度的关系是解本题关键,注意:无论水的电离程度多大,水不能变为酸或碱,仍然呈中性,题目较简单.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
16.能将分别含有Cu2+、Fe3+、Al3+、Fe2+、Mg2+、NH4+、Na+等离子的七种溶液一次鉴别出来的试剂是( )
| A. | NaHCO3溶液 | B. | KSCN溶液 | C. | NaOH溶液 | D. | NH3•H2O溶液 |
1.已知碳碳单键可以绕键轴旋转,关于结构简式可表示为的烃,下列说法中正确的是( )


| A. | 分子中至少有4个碳原子处于同一直线上 | |
| B. | 该烃苯环上的一氯代物有4种 | |
| C. | 分子中至少有10个碳原子处于同一平面上 | |
| D. | 该烃是苯的同系物 |
11.如表所示的五种元素中,甲、乙、丙、丁为短周期元素,其中乙是地壳中含量最多的元素.下列说法正确的是
( )
( )
| 甲 | 乙 | ||
| 丙 | 丁 | ||
| 戊 |
| A. | 原子半径:甲>乙 | |
| B. | 丁和戊的原子核外电子数相差8 | |
| C. | 最高价氧化物对应的水化物的酸性:丙>丁 | |
| D. | 甲的单质在空气中燃烧生成只含共价键的化合物 |
18.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1mol•L-1的溶液中Na+、SiO32-、I-、CO32- | |
| B. | 2%的氨水中Ag+、K+、F-、NO3- | |
| C. | pH=1的溶液中NH4+、Na+、SO42-、C17H35COO- | |
| D. | 0.1mol•L-1的NaHSO4溶液中K+、Fe2+、Cl-、CrO42- |
13.将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).
实验测得不同温度下的平衡数据列于下表:
(1)可以判断该分解反应已经达到化学平衡状态的是BC.
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
(2)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量将增加(填“增加”“减小”或“不变”).
(3)氨基甲酸铵分解反应的焓变△H>0,熵变△S>0(填“>”“<”或“=”).
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3 mol•L-1) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
(2)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量将增加(填“增加”“减小”或“不变”).
(3)氨基甲酸铵分解反应的焓变△H>0,熵变△S>0(填“>”“<”或“=”).
 ②
②
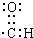 ③
③
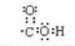 ④-C≡C-
④-C≡C- .
.