题目内容
将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g) + Y(g)  2Z(g);△H < 0。当改变某一条件并达到新平衡后,下列叙述正确的是
2Z(g);△H < 0。当改变某一条件并达到新平衡后,下列叙述正确的是
 2Z(g);△H < 0。当改变某一条件并达到新平衡后,下列叙述正确的是
2Z(g);△H < 0。当改变某一条件并达到新平衡后,下列叙述正确的是| A.缩小容器体积,Z的浓度不变 |
| B.升高温度,X的转化率增大 |
| C.保持容器体积不变,充入一定量的氦气,Y的浓度不变 |
| D.保持压强不变,再充入0.2 mol X和0.2 mol Y,X的体积分数增大 |
C
略

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
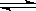 2SO3 (g);△H=-a kJ·mol-1在相同条件下,要想得到2a kJ热量,加入各物质的物质的量可能是
2SO3 (g);△H=-a kJ·mol-1在相同条件下,要想得到2a kJ热量,加入各物质的物质的量可能是 2NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2 )= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则:
2NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2 )= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则: Y(g)+Z(s),
Y(g)+Z(s),
 2AB3(g)化学平衡状态的影响时,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的结论正确的是 ( )
2AB3(g)化学平衡状态的影响时,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的结论正确的是 ( )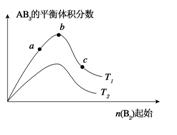
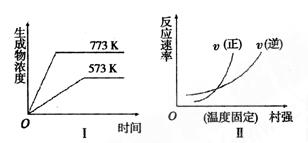
 2NH3(g)ΔH<0
2NH3(g)ΔH<0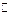 2SO3中,当SO2、O2、SO3三者物质的量之比为2∶1∶2时表示已达平衡状态的标志
2SO3中,当SO2、O2、SO3三者物质的量之比为2∶1∶2时表示已达平衡状态的标志 CO2(g)+H2(g),达到平衡时测得n(H2)为0.5mol,下列说法不正确的是 ( )
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5mol,下列说法不正确的是 ( )