题目内容
(15分)某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
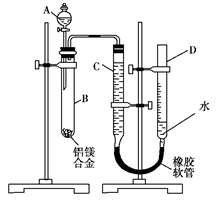
(1)A中试剂为 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是______________
___________________________________________________________。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤、洗涤、干燥、称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B中滴加足量试剂;⑤检查气密性。上述操作的顺序是 (填序号);记录C的液面位置时,除视线平视外,还应__________________ 。
(4)B中发生反应的化学方程式为__________________________ 。
(5)若实验用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固体的质量为c g,则铝的相对原子质量为 。
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将 。(填“偏大”、“偏小”、“不受影响”)

(1)A中试剂为 。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是______________
___________________________________________________________。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤、洗涤、干燥、称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B中滴加足量试剂;⑤检查气密性。上述操作的顺序是 (填序号);记录C的液面位置时,除视线平视外,还应__________________ 。
(4)B中发生反应的化学方程式为__________________________ 。
(5)若实验用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固体的质量为c g,则铝的相对原子质量为 。
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将 。(填“偏大”、“偏小”、“不受影响”)
(1)NaOH溶液 (2)除去铝镁合金表面的氧化膜
(3)⑤①④③② 使D和C的液面相平 (4)2Al+2NaOH+2H2O===2NaAlO2+3H2↑
(5)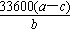 (6)偏小
(6)偏小
(3)⑤①④③② 使D和C的液面相平 (4)2Al+2NaOH+2H2O===2NaAlO2+3H2↑
(5)
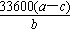 (6)偏小
(6)偏小】(1)Mg、Al均可以和酸反应,因此不可以用酸来实验,由于Al可以和碱反应而不和Mg反应,则可以用NaOH与Al反应制得H2,然后用排水法收集H2,以计算Al的量。(2)由于Al表面容易生成氧化膜,因而要用酸处理。(3)整个操作过程及原理是:检查气密性;记录起始液面;加入碱反应;不产生气体后,记录未读数,两将相减即为产生H2的量;最后称得的固体即为Mg的质量。在读数时要注意D、C液面相平,否则气体将受压,超成读数不准。(4)B中发生的是Al与碱的反应;(5)(a-c)即为铝的质量,再除以Al的物质的量即为铝的摩尔质量。而n(Al)可以由产生的H2获得;(6)未洗涤,则超成(a-c)变小,则由(5)的结果得,偏小

练习册系列答案
相关题目