题目内容
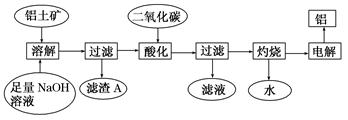
(10分)(一)铝是生活中非常常见的一种金属,运用所学知识回答:
(1)金属铝是活泼的金属,但在生活中应用很广泛,原因是 。
(2)铝盐或铁盐能用于净水,是因为铝盐或铁盐在水溶液中形成了 。
(3)铝粉与氧化铁粉末在高温下得到铁的反应叫做“铝热反应”,发生反应的化学方程式为 。
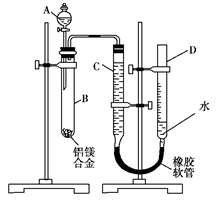
(二)有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸。某研究性学习小组的同学们利用一小块样品,设计实验证明矿物样品中有Fe3+。
实验用品:研钵、烧杯、玻璃棒、漏斗、铁架台、滤纸、试管、胶头滴管
(4)简述实验操作步骤、现象和结论。
(1)金属铝是活泼的金属,但在生活中应用很广泛,原因是 。
(2)铝盐或铁盐能用于净水,是因为铝盐或铁盐在水溶液中形成了 。
(3)铝粉与氧化铁粉末在高温下得到铁的反应叫做“铝热反应”,发生反应的化学方程式为 。
(二)有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸。某研究性学习小组的同学们利用一小块样品,设计实验证明矿物样品中有Fe3+。
实验用品:研钵、烧杯、玻璃棒、漏斗、铁架台、滤纸、试管、胶头滴管
(4)简述实验操作步骤、现象和结论。
(1)铝表面容易生成一层致密的氧化物保护膜,对内部的金属起到了保护作用
(2)胶体
(3)2Al+Fe2O3 2Fe+Al2O3
2Fe+Al2O3
(4)将样品在研钵中研细,倒入烧杯,加入稀硫酸,搅拌,过滤,取少许溶液,滴加KSCN溶液,若溶液变为红色,则证明矿物样品中有 ,不变红,则无。
(2)胶体
(3)2Al+Fe2O3
 2Fe+Al2O3
2Fe+Al2O3(4)将样品在研钵中研细,倒入烧杯,加入稀硫酸,搅拌,过滤,取少许溶液,滴加KSCN溶液,若溶液变为红色,则证明矿物样品中有 ,不变红,则无。
本大题第(一)题属基础知识题,考查对相关知识的识记、再现。第(二)题是据提供的用品和相关原理及实验自行设计实验进行一种离子(Fe3+)的检验,考查相关实验操作、基本设计和表达能力,实验方法常用并已知,而提供的用品也能提示就是使用该方法,所以难度一般。实验步骤在检验之前须有对样品的预处理,即研碎、酸溶、过滤,这要求学生须有相关实验的经验和知识。

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目