题目内容
【题目】易混易错题组
(1)在一定温度下的定容容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的浓度之比等于化学计量数之比,⑦某种气体的百分含量
①能说明2SO2(g)+O2(g) ![]() 2SO3(g)达到平衡状态的是________。
2SO3(g)达到平衡状态的是________。
②能说明I2(g)+H2(g) ![]() 2HI(g)达到平衡状态的是________。
2HI(g)达到平衡状态的是________。
③能说明C(s)+CO2(g) ![]() 2CO(g)达到平衡状态的是________。
2CO(g)达到平衡状态的是________。
④能说明NH2COONH4(s) ![]() 2NH3(g)+CO2(g)达到平衡状态的是________。
2NH3(g)+CO2(g)达到平衡状态的是________。
(2)对于以下三个反应,从正反开始进行达到平衡后,保持温度、体积不变,按要求回答下列问题。
①PCl5(g) ![]() PCl3(g)+Cl2(g),再充入PCl5(g)平衡向________方向移动,达到平衡后,PCl5(g)的转化率_____,PCl5(g)的百分含量______。
PCl3(g)+Cl2(g),再充入PCl5(g)平衡向________方向移动,达到平衡后,PCl5(g)的转化率_____,PCl5(g)的百分含量______。
②2HI(g) ![]() I2(g)+H2(g),再充入HI(g)平衡向________方向移动,达到平衡后,HI的分解率________,HI的百分含量________。
I2(g)+H2(g),再充入HI(g)平衡向________方向移动,达到平衡后,HI的分解率________,HI的百分含量________。
③2NO2(g) ![]() N2O4(g),再充入NO2(g),平衡向________方向移动,达到平衡后,NO2(g)的转化率________,NO2(g)的百分含量________。
N2O4(g),再充入NO2(g),平衡向________方向移动,达到平衡后,NO2(g)的转化率________,NO2(g)的百分含量________。
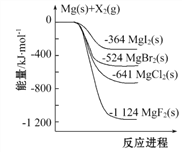
(3)一定的条件下,合成氨反应为:N2(g)+3H2(g)![]() 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。

①该反应的平衡常数表达式为_______,升高温度,平衡常数______(填“增大”或“减小”或“不变”)。
②由图2分析,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为______(填“a”或“b”或“c”或“d”)。
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是___点,温度T1____T2(填“>”或“=”或“<”)。
【答案】①③④⑦ ⑤⑦①②③④⑦①②③正反应减小增大正反应不变不变正反应增大减小![]() 减小dc<
减小dc<
【解析】
(1)(I)对于反应2SO2(g)+O2(g)2SO3(g),①混合气体的压强,说明气体的物质的量不变,反应达平衡状态,故正确;②混合气体的密度一直不变,故错误;③混合气体的总物质的量不变,反应达平衡状态,故正确;④混合气体的平均相对分子质量,说明气体的物质的量不变,反应达平衡状态,故正确;⑤混合气体的颜色一直不变,反应达平衡状态,故错误;⑥只要反应发生就有各反应物或生成物的反应速率之比等于化学计量数之比,故错误;⑦某种气体的百分含量不变,说明各物质的量不变,反应达平衡状态,故正确;故答案为:①③④⑦;
(Ⅱ)I2(g)+H2(g)2HI(g)反应前后两边计量数相等,①混合气体的压强一直不变,所以不一定达平衡状态,故错误;②混合气体的密度一直不变,所以不一定达平衡状态,故错误;③混合气体的总物质的量,一直不变,所以不一定达平衡状态,故错误;④混合气体的平均相对分子质量,一直不变,所以不一定达平衡状态,故错误;⑤混合气体的颜色,说明碘蒸气的浓度不变反应达平衡状态,故正确;⑥各反应物或生成物的浓度之比等于系数之比,不能说明各物质的量不变,所以不一定达平衡状态,故错误;⑦某种气体的百分含量不变,说明各物质的量不变,反应达平衡状态,故正确;故答案为:⑤⑦;
(Ⅲ)反应C(s)+CO2(g)2CO(g),①混合气体的压强,说明气体的物质的量不变,反应达平衡状态,故正确;②混合气体的密度,说明气体的物质的量不变,反应达平衡状态,故正确;③混合气体的总物质的量,正逆反应速率相等反应达平衡状态,故正确;④混合气体的平均相对分子质量,正逆反应速率相等反应达平衡状态,故正确;⑤混合气体的颜色一直不变,反应不一定达平衡状态,故错误;⑥各反应物或生成物的浓度之比等于系数之比,不能说明各物质的量不变,所以不一定达平衡状态,故错误;⑦某种气体的百分含量,说明各物质的量不变,反应达平衡状态,故正确;故选:①②③④⑦;
(Ⅳ)反应NH2COONH4(s)2NH2(g)+CO2(g),①混合气体的压强,说明气体的物质的量一定,反应达平衡状态,故正确;②混合气体的密度,说明气体的质量一定反应达平衡状态,故正确;③混合气体的总物质的量,说明正逆反应速率相等,反应达平衡状态,故正确;④混合气体的平均相对分子质量,一直不变,所以不一定达平衡状态,故错误;⑤混合气体的颜色一直不变,所以不一定达平衡状态,故错误;⑥各反应物或生成物的浓度之比等于系数之比一直不变,所以不一定达平衡状态,故错误;⑦某种气体的百分含量一直不变,所以不一定达平衡状态,故错误;故选:①②③。
(2)①PCl5(g) ![]() PCl3(g)+Cl2(g),保持温度、体积不变,再充入PCl5(g),平衡正向移动,该反应为气体体积增大的反应,充入PCl5(g),相当于增大压强,增大压强,与原平衡相比,平衡逆向移动,PCl5(g)的转化率减小,PCl5(g)的百分含量增大,故答案为:正反应;减小;增大;
PCl3(g)+Cl2(g),保持温度、体积不变,再充入PCl5(g),平衡正向移动,该反应为气体体积增大的反应,充入PCl5(g),相当于增大压强,增大压强,与原平衡相比,平衡逆向移动,PCl5(g)的转化率减小,PCl5(g)的百分含量增大,故答案为:正反应;减小;增大;
②2HI(g) ![]() I2(g)+H2(g),恒温恒容条件下,再充入HI(g),HI浓度增大,平衡正向移动,充入HI(g),压强增大,2HI(g)I2(g)+H2(g)前后气体系数和相等,压强不影响平衡移动,达到平衡后,HI的分解率不变,HI的百分含量不变;故答案为:正反应;不变;不变;
I2(g)+H2(g),恒温恒容条件下,再充入HI(g),HI浓度增大,平衡正向移动,充入HI(g),压强增大,2HI(g)I2(g)+H2(g)前后气体系数和相等,压强不影响平衡移动,达到平衡后,HI的分解率不变,HI的百分含量不变;故答案为:正反应;不变;不变;
③恒温恒容,达平衡后再充入NO2气体,NO2浓度增大,平衡正向移动,再充入NO2气体,相当给原平衡体系增加压强,平衡正向移动,到达平衡后,NO2(g)的转化率增大,NO2(g)的百分含量减小,故答案为:正反应;增大;减小;
(3)①N2(g)+3H2(g)2NH3(g)的平衡常数K=![]() ,由图1可知,反应物总能量大于生成物能量,正反应为放热反应,升高温度平衡逆向移动,平衡常数减小,故答案为:
,由图1可知,反应物总能量大于生成物能量,正反应为放热反应,升高温度平衡逆向移动,平衡常数减小,故答案为:![]() ;减小;
;减小;
②从11min起其它条件不变,压缩容器的体积为1L,压强增大,瞬间氮气的物质的量不变,增大压强,平衡正向移动,氮气物质的量减小到平衡时不变,曲线d符合n(N2)的变化,故答案为: d;
③图3表示平衡时氨气含量与氢气起始物质的量关系,曲线上各点都处于平衡状态,故a、b、c都处于平衡状态,达平衡后,增大氢气用量,氮气的转化率增大,故a、b、c三点中,c的氮气的转化率最高;由图3可知,氢气的起始物质的量相同时,温度T1平衡后,氨气的含量更高,该反应为放热反应,降低温度平衡向正反应移动,故温度T1<T2,故答案为:c;<。

 优加精卷系列答案
优加精卷系列答案【题目】下列实验不能达到实验目的的是_________________。
序号 | 实验内容 | 实验目的 |
A | 盛有 | 探究浓度对反应速率的影响 |
B | 一定条件下,分别在容积为1 L和容积为2 L的两个密闭容器中加入等量的氢气和碘蒸气,发生如下反应: H2(g)+I2(g) | 当其他条件不变时,气态反应体系的压强越大,化学反应速率越快 |
C | 在容积可变的密闭容器中发生反应:2NO2(g) | 正反应速率加快,逆反应速率也加快 |
D | 向2支试管中各加入相同体积、相同浓度的 | 探究温度对反应速率的影响 |