题目内容
【题目】下图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是( )
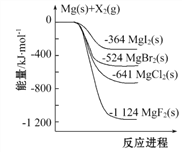
A. 由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方 程式为:MgBr2(s)+Cl2(g)![]() MgCl2(s)+Br2(g) ΔH=+117 kJ·mol-1
MgCl2(s)+Br2(g) ΔH=+117 kJ·mol-1
B. 热稳定性: MgI2 > MgBr2 > MgCl2 > MgF2
C. 工业上可由电解MgCl2溶液冶炼金属Mg,该过程需吸收热量
D. 金属镁和卤素单质(X2)的反应能自发进行是因为ΔH均小于零
【答案】D
【解析】
A. 由图可知此温度下MgBr2(s)与Cl2(g)反应是放热反应,热化学方程式为:MgBr2(s)+Cl2(g)![]() MgCl2(s)+Br2(g) ΔH=-117 kJ·mol-1,故A错误;B、物质具有的能量越低越稳定,由图可知 热稳定性: MgI2< MgBr2 < MgCl2 < MgF2,故B错误;C、已知由镁制取氯化镁是放热过程,所以电解熔融氯化镁制取镁单质是是吸热过程,而电解MgCl2溶液不能得到镁单质,故C错误;D、根据图像可知,反应物总能量大于生成物总能量,均为放热反应,ΔH均小于零,能自发进行,故D正确;故选D。
MgCl2(s)+Br2(g) ΔH=-117 kJ·mol-1,故A错误;B、物质具有的能量越低越稳定,由图可知 热稳定性: MgI2< MgBr2 < MgCl2 < MgF2,故B错误;C、已知由镁制取氯化镁是放热过程,所以电解熔融氯化镁制取镁单质是是吸热过程,而电解MgCl2溶液不能得到镁单质,故C错误;D、根据图像可知,反应物总能量大于生成物总能量,均为放热反应,ΔH均小于零,能自发进行,故D正确;故选D。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目


