题目内容
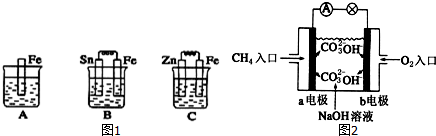
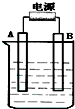 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题:(1)A接的是电源的
(2)写出电解时反应的总离子方程式
(3)电解后溶液的pH值为
考点:电解原理,原电池和电解池的工作原理
专题:电化学专题
分析:溶液呈蓝色说明含有铜离子,用石墨作电极电解铜盐溶液时,A电极上有红色金属单质铜生成,说明A为阴极,则B为阳极,阳极上有无色气体生成,说明B电极上氢氧根离子放电,该溶液为铜的含氧酸盐溶液,根据“析出什么加入什么”的原则加入物质使溶液恢复原状.
解答:
解:溶液呈蓝色说明含有铜离子,用石墨作电极电解铜盐溶液时,A电极上有红色金属单质铜生成,说明A为阴极,则B为阳极,阳极上有无色气体生成,说明B电极上氢氧根离子放电,该溶液为铜的含氧酸盐溶液,
(1)通过以上分析知,A是阴极,接电源负极,故答案为:负;
(2)电解时,阴极上铜离子放电、阳极上氢氧根离子放电,所以电池反应式为2Cu2++2H2O
Cu+O2↑+4H+,故答案为:2Cu2++2H2O
Cu+O2↑+4H+;
(3)根据2Cu2++2H2O
Cu+O2↑+4H+知,电解时生成氢离子,导致溶液酸性增强,溶液的pH减小,阳极上生成氧气、阴极上生成铜,实质上相当于生成CuO,要使溶液恢复原状,应该加入CuO,根据Cu原子守恒得m(CuO)=
×80g/mol=2g,
故答案为:减小;CuO;2g.
(1)通过以上分析知,A是阴极,接电源负极,故答案为:负;
(2)电解时,阴极上铜离子放电、阳极上氢氧根离子放电,所以电池反应式为2Cu2++2H2O
| ||
| ||
(3)根据2Cu2++2H2O
| ||
| 1.6g |
| 64g/mol |
故答案为:减小;CuO;2g.
点评:本题考查了电解原理,根据阴阳极上得失电子确定溶液酸碱性变化,再结合原子守恒进行计算,题目难度不大.

练习册系列答案
相关题目
下列不可用于区别溴蒸气与二氧化氮气体的试剂是( )
| A、淀粉碘化钾溶液 |
| B、水 |
| C、AgNO3溶液 |
| D、CCl4 |
不能用于鉴别甲烷和乙烯的试剂是( )
| A、溴的四氯化碳溶液 |
| B、酸性高锰酸钾溶液 |
| C、苛性钠溶液 |
| D、溴水 |
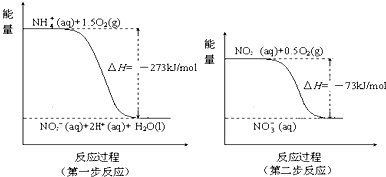
 为了研究碳酸钙与盐酸反应的反应速率,某同学通过如图实验装置测定反应中生成的CO2气体体积,并绘制出如图所示的曲线.请分析讨论以下问题.
为了研究碳酸钙与盐酸反应的反应速率,某同学通过如图实验装置测定反应中生成的CO2气体体积,并绘制出如图所示的曲线.请分析讨论以下问题.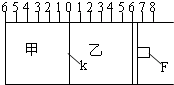 (Ⅰ)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g); 反应达到平衡后,再恢复至原温度.回答下列问题:
(Ⅰ)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g); 反应达到平衡后,再恢复至原温度.回答下列问题: