题目内容
短周期元素X、Y、Z的原子序数依次增大,Y为ⅠA族元素,X与Z同主族,3种元素原子的最外层电子数之和为13,下列判断正确的是( )
| A.Y元素位于第2周期 | B.Y、Z均能与X形成不只一种化合物 |
| C.X是VA族元素 | D.氢化物的稳定性:HnZ > HnX |
B
解析试题分析:根据题意可知:X是O;Y是Na;Z是S。A.Na在周期表中位于第三周期第ⅠA族。错误。B.Na、O可以形成Na2O、Na2O2两种氧化物;S、O可以形成SO2、SO3形成不只一种化合物。正确。C.O是第VIA族的元素。错误。D.O、S是同一主族的元素,由于非金属性O>S。元素的非金属性越强,其氢化物的稳定性就越强,因此稳定性H2O>H2S。错误。
考点:考查元素的推断及元素的结构、位置、性质的关系的知识。

练习册系列答案
相关题目
下列判断正确的是
| A.根据同周期元素的第一电离能变化趋势,推出P的第一电离能比S大 |
| B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正化合价都是+7 |
| C.晶体中一定存在化学键 |
| D.正四面体分子中键角只能是109°28′ |
位于同一周期的三种短周期元素X、Y、Z,它们的最高价氧化物分别为酸性氧化物、碱性氧化物和两性氧化物,则三种元素的原子序数的大小顺序是
| A.X>Y>Z | B.Y>Z>X | C.X>Z>Y | D.Z>X>Y |
19世纪门捷列夫的突出贡献是
| A.提出了原子学说 | B.提出了分子学说 |
| C.发现了稀有气体 | D.发现了元素周期律 |
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,其最外层电子数之和等于24,由此可知说法错误的是( )
| W | X | |
| | Y | Z |
A.原子半径大小:W>X
B.元素最高正价:W>Z
C.简单阴离子的还原性:Y>Z
D.气态氢化物的稳定性:X>Y
短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2molECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀。下列判断错误的是
| A.E可能是一种金属元素 |
| B.在ECln中E与Cl之间形成共价键 |
| C.E位于元素周期表的IVA族 |
| D.E的一种氧化物为EO |
下列关于元素周期表的说法中正确的是
| A.元素周期表有8个主族 |
| B.ⅠA族的元素全部是金属元素 |
| C.元素周期表有7个周期 |
| D.短周期是指第1、2周期 |
下列说法正确的是
| A.非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价 |
| B.只有非金属能形成含氧酸或含氧酸盐 |
| C.除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| D.非金属的最高价含氧酸都具有强氧化性 |
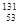 I是常规核裂变产物之一,可以通过测定大气或水中
I是常规核裂变产物之一,可以通过测定大气或水中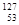 相同 B
相同 B