题目内容
15.短周期主族X、Y、Z、W、Q的原子序数依次增大,X+中只含有1个质子,Y原子的最外层电子数是内层电子数的2倍,Z 和 Q同主族且能形成两种常见化合物QZ2、QZ3,W是短周期中原子半径最大的元素.下列叙述正确的是( )| A. | Y3X8分子中,极性键和非极性键的个数比为8:3 | |
| B. | Z和Q形成的两种化合物中只有一种属于酸性氧化物 | |
| C. | 25℃时,若WZX溶液中的C(OH-):C(H+)=1012,则该溶液的pH=13 | |
| D. | Q元素在自然界中不能以游离态存在 |
分析 短周期主族X、Y、Z、W、Q的原子序数依次增大,X+中只含有1个质子,则X为H元素;Y原子的最外层电子数是内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故Y为C元素;W是短周期中原子半径最大的元素,则W为Na;Z 和 Q同主族且能形成两种常见化合物QZ2、QZ3,则Z为O元素、Q为S元素,据此解答.
解答 解:短周期主族X、Y、Z、W、Q的原子序数依次增大,X+中只含有1个质子,则X为H元素;Y原子的最外层电子数是内层电子数的2倍,原子只能有2个电子层,最外层电子数为4,故Y为C元素;W是短周期中原子半径最大的元素,则W为Na;Z 和 Q同主族且能形成两种常见化合物QZ2、QZ3,则Z为O元素、Q为S元素.
A.C3H8分子中,C-C键为非极性键,C-H键为极性键,极性键和非极性键的个数比为8:2,故A错误;
B.Z和Q形成的两种化合物SO2、SO3,均属于酸性氧化物,故B错误;
C.25℃时,若NaOH溶液中的c(OH-):c(H+)=1012,结合c(OH-)×c(H+)=10-14,可知c(H+)=10-13mol/L,则该溶液的pH=-lg10-13=13,故C正确;
D.火山喷发口存在单质硫,故D错误,
故选C.
点评 本题考查结构性质位置关系应用,难度不大,推断元素是解题关键,注意基础知识的掌握.

练习册系列答案
相关题目
1.用下列实验装置进行相应实验,能达到实验目的是( )


| A. | 用图1所示装置可收集NO气体 | |
| B. | 用图4装置可证明酸性:H2SO4>H2CO3>H2SiO3 | |
| C. | 用图3所示装置可实现反应:2H2O$\frac{\underline{\;电解\;}}{\;}$O2↑+H2↑ | |
| D. | 用图2所示装置可吸收多余氨气且能防止倒吸 |
6.下列有关说法中,正确的是( )
| A. | 糖类、油脂和蛋白质都是天然高分子化合物 | |
| B. | 用福尔马林(甲醛溶液)浸泡海产品,可长时间保鲜 | |
| C. | 粮食酿酒主要经过淀粉→葡萄糖→乙醇的化学变化过程 | |
| D. | 明矾既可用于净水,也可杀菌消毒 |
3.某药物中间体的合成路线如下:下列说法正确的是( )
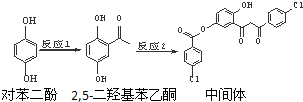

| A. | 对苯二酚和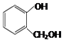 互为同系物 互为同系物 | |
| B. | 1 mol该中间体最多可与7 mol氢氧化钠反应 | |
| C. | 2,5-二羟基苯乙酮能发生加成、水解等反应 | |
| D. | 该中间体分子含有羰基和羟基两种含氧官能团 |
10.下列反应的离子方程式书写正确的是( )
| A. | 向次氯酸钙溶液中通入SO2:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO | |
| B. | Fe3O4与稀硝酸反应:Fe3O4+8H+=2Fe2++Fe3++4H2O | |
| C. | 大理石溶于醋酸中:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | 溶液中FeBr2与等物质的量的Cl2反应:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+Br2 |
20.短周期主族元素A、B、C、D、E的原子序数依次增大,其中A与C同主族,A与其它元素不在同一周期,B与D同主族,常温下D的单质为淡黄色固体.下列推断正确的是( )
| A. | 原子半径由小到大的顺序:r(C)<r(D)<r(E) | |
| B. | 元素D、E分别与A形成的化合物的热稳定性:E>D | |
| C. | 元素D的最高价氧化物对应水化物的酸性比E的强 | |
| D. | 元素B分别与A、C形成的化合物中化学键的类型不同 |
7.化学与生产、生活密切相关,下列说法错误的是( )
| A. | 雾霾可能是许多组小液体和固体微粒分散到空气中形成的一种气溶胶 | |
| B. | 福尔马林可浸制标本,利用了其使蛋白质变性的性质 | |
| C. | 含磷合成洗涤剂易被细菌分解,故不会导致水体污染 | |
| D. | 大量使用风能、太阳能、符合“低碳”概念 |
4.密闭的真空容器中放入一定量CaO2固体,发生反应2CaO2(s)?2CaO(s)+O2(g)并达到平衡.保持温度不变,缩小容器容积为原来的三分之二,重新平衡后,下列叙述正确的是( )
| A. | 平衡常数减小 | B. | CaO的量减少 | C. | 氧气浓度不变 | D. | CaO2的量不变 |