题目内容
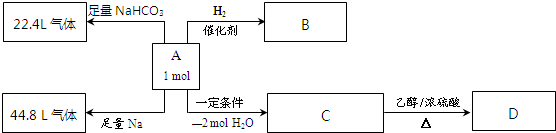
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质,已知,它们可以发生如下反应:甲+乙→丁+己,甲+丙→戊+己;0.1mol/L丁溶液的pH为13(25℃).它们满足如图转化关系,下列说法正确的是( )
| A、Z元素在周期表中的位置为二周期第ⅥA族 |
| B、原子半径:W>Z>Y>X |
| C、1mol甲与足量的乙完全反应共转移了2mol电子 |
| D、1L 0.1mol/L戊溶液中阴离子总的物质的量小于0.1mol |
考点:无机物的推断
专题:推断题,元素周期律与元素周期表专题
分析:0.1mol/L丁溶液的pH为13,说明丁为强碱,应为NaOH,甲和乙反应生成强碱和单质,则应为过氧化钠和水的反应,可知己为氧气,Z为O元素,而甲和丙反应也生成氧气,则可知甲为Na2O2,乙为H2O,丙为CO2,戊为Na2CO3,结合原子序数关系可知X为H元素,Y为C元素,Z为O元素,W为Na元素,以此解答该题.
解答:
解:0.1mol/L丁溶液的pH为13,说明丁为强碱,应为NaOH,甲和乙反应生成强碱和单质,则应为过氧化钠和水的反应,可知己为氧气,Z为O元素,而甲和丙反应也生成氧气,则可知甲为Na2O2,乙为H2O,丙为CO2,戊为Na2CO3,结合原子序数关系可知X为H元素,Y为C元素,Z为O元素,W为Na元素,
A.Z为O元素,位于周期表二周期第ⅥA族,故A正确;
B.原子半径W(Na)>Y(C)>Z(O)>X(H),故B错误;
C.1mol甲与足量的乙完全反应,发生2Na2O2+2H2O=4NaOH+O2↑,O元素化合价由-1价分别变化为0价、-2价,则完全反应共转移了1mol电子,故C错误;
D.戊为Na2CO3,CO32-可水解生成HCO3-和OH-,阴离子物质的量增大,故D错误.
故选A.
A.Z为O元素,位于周期表二周期第ⅥA族,故A正确;
B.原子半径W(Na)>Y(C)>Z(O)>X(H),故B错误;
C.1mol甲与足量的乙完全反应,发生2Na2O2+2H2O=4NaOH+O2↑,O元素化合价由-1价分别变化为0价、-2价,则完全反应共转移了1mol电子,故C错误;
D.戊为Na2CO3,CO32-可水解生成HCO3-和OH-,阴离子物质的量增大,故D错误.
故选A.
点评:本题综合考查元素周期律以及无机物的推断,侧重于学生的分析能力的考查,注意把握物质的相关性质,找出题目的突破口,难度中等.

练习册系列答案
相关题目
下列叙述正确的是( )
A、因为Na2CO3+SiO2
| ||||
| B、碳和硅都是ⅣA族的元素,所以二氧化碳和二氧化硅的物理性质相似 | ||||
| C、二氧化硅既溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物 | ||||
| D、二氧化硅是酸的酸酐,但不与水反应产生硅酸 |
下列说法中不正确的是( )
| A、二十碳五烯酸和二十二碳六烯酸是鱼油的主要成分,它们含有相同的官能团,是同系物,化学性质相似 |
| B、分子式为C4H8Br2结构中含一个一CH3的同分异构体(不考虑立体异构)有4种 |
C、结构简式为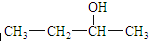 的有机物其名称为2-丁醇 的有机物其名称为2-丁醇 |
| D、对苯二甲酸和1,4-丁二醇作用形成的聚合物的链节中只含有一个苯环 |
下列氢氧化物中,碱性最强的是( )
| A、KOH |
| B、NaOH |
| C、Mg(OH)2 |
| D、Al(OH)3 |
下列说法正确的是( )
| A、硅和石墨都是重要的半导体材料 |
| B、SO2、NO2、CO2都会导致酸雨的形成 |
| C、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理不同 |
| D、氢能是清洁能源,工业上用电解水法制大量氢气符合节能减排理念 |
金刚石和石墨是碳元素的两种结构不同的单质(同素异形体).在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热能.据此判断在100kPa压强下,下列结论正确的是( )
| A、石墨比金刚石稳定 |
| B、金刚石比石墨稳定 |
| C、1mol石墨比1mol金刚石的总能量高 |
| D、1mol石墨比1mol金刚石的总能量低 |
下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最快的是( )
| A、10℃10mL 4mol/L的盐酸溶液 |
| B、20℃10mL 4mol/L的盐酸溶液 |
| C、20℃20mL 2mol/L的盐酸溶液 |
| D、20℃40mL 2mol/L的盐酸溶液 |